题目内容
【题目】水是宝贵的自然资源。请根据下列情况回答问题。
(1)淡水资源有限,我们需要节约用水,图中表示节水标志的是______。

(2)电解水反应前后不变的微粒是______(写微粒符号)。
(3)要除去水样中的色素和异味通常加入活性炭,是利用其具有______性。
【答案】B H、O 吸附
【解析】
电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2,质量比是8:1,电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的。
(1)图中表示节水标志的是B。
(2)根据质量守恒定律,反应前后原子个数不变,故电解水反应前后不变的微粒是H、O。
(3)活性炭能够吸附色素、异味,要除去水样中的色素和异味通常加入活性炭,是利用其具有吸附性。

 津桥教育计算小状元系列答案
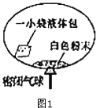
津桥教育计算小状元系列答案【题目】某研究小组对自动充气气球(如图1)进行下探究。
(查阅资料)
①该气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧 化碳气体,实现气球自动充气。
②氯化钙水溶液呈中性,碳酸钠、碳酸氢钠的水溶液均呈碱性。
③用一定溶质质量分数的 NaHCO3和Na2CO3溶液进行实验,实验现象记录如下:
NaHCO3溶液 | Na2CO3溶液 | |
加入澄清石灰水 | 溶液变浑浊 | 溶液变浑浊 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
加热溶液至沸腾,将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
探究1:气体的成分
为检验气体是二氧化碳,可选用______(填试剂名称).
探究2:液体包内溶液的酸碱性
室温时,用 pH试纸测得溶液的 pH 的方法是____;若 测得溶液的 pH=3,则该溶液呈___性。
探究 3:白色粉末的成分
(猜想与假设)甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学 认为是碳酸钠和碳酸氢钠的混合物。
(进行实验)
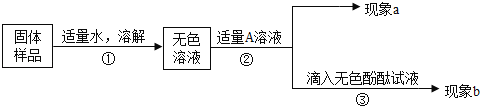
(1)将少量白色粉末放入水中搅拌,观察到______,说明甲同学的猜想不正确。
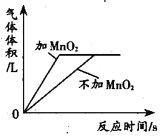
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的
10%的盐酸(装置如图2),记录如下表:


(解释与结论)
(1)实验Ⅰ的化学方程式为__________。
(2)表中a=_______;V1________V2(填“>”、“<”或“=”)。
(3)上述实验得出的结论及判断依据是__________。
(反思与评价)老师指出还可以采用更简单的方法得出与上述实验(2)相同的结论,实验方案为____。