题目内容
【题目】兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。
请你与他们一起完成以下探究活动:
(对固体猜想)
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:是_____。
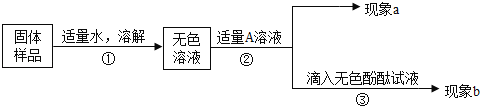
(实验和推断)
(1)若现象a为有气泡产生,则加入的A溶液是_____,说明氢氧化钠已经变质。
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,该实验_____(填“能”或“不能”)说明样品中有NaOH。
(3)若A是CaCl2溶液,当实验现象a为_____,现象b为_____,则猜想Ⅱ成立。
(反思)久置的氢氧化钠变质的原因是_____(用化学方程式表示)。
【答案】Na2CO3和NaOH的混合物 稀盐酸 不能 有白色沉淀产生 无色酚酞不变红色 CO2+2NaOH=Na2CO3+H2O
【解析】
猜想Ⅲ:已知空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水,因此做出的三个猜想是:全部是NaOH;全部是Na2CO3;Na2CO3和NaOH的混合物;故答案为:Na2CO3和NaOH的混合物;
[实验和推断](1)若现象a为有气泡产生,则加入的A溶液是稀盐酸或稀硫酸,说明氢氧化钠已经变质,故答案为:稀盐酸;
(2)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为碳酸钙,该实验不能说明样品中有氢氧化钠,因为碳酸钠和氢氧化钙反应会生成氢氧化钠;故答案为:不能;
(3)若A是氯化钙溶液,现象a有白色沉淀产生,现象b无色酚酞不变红色,则猜想Ⅱ成立,因为碳酸钠和氯化钙反应生成碳酸钙白色沉淀和氯化钠,氯化钠显中性;故答案为:有白色沉淀产生,无色酚酞不变红色;
[反思]久置的氢氧化钠变质的原因是:空气中的二氧化碳与氢氧化钠反应生成碳酸钠和水,故答案为:CO2+2NaOH=Na2CO3+H2O。

【题目】化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊。
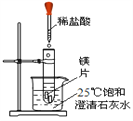
(一)石灰水变浑浊的原因是:
(1)镁和盐酸的反应________(填“吸热”或“放热”)。
(2)_____________________________________________。
(二)甲同学测得反应后试管内溶液pH<7 ,该溶液pH<7的可能原因是:
①MgCl2溶液的pH<7; ②__________________________。
(三)乙同学将反应后试管内溶液冷却,加入镁粉并滴入酚酞,溶液颜色无变化,再加热,发现溶液慢慢浑浊且变红。
【猜想】对实验中“溶液慢慢浑浊且变红”的原因,乙同学提出猜想:
MgCl2+2H2O=Mg(OH)2↓+2HCl,大家都认为此猜想不合理,理由是_________。
【查阅】资料1:Mg(OH)2难溶解于水,升高温度可加大其在水中的溶解度。
资料2:K、Ca、Na、Mg等活泼金属在一定条件下能与水反应,产生碱和气体。
【实验】乙同学重新在滴有酚酞的热水中加入镁粉,观察到液体慢慢变红并浑浊,镁粉表面产生气泡。收集并点燃气体,发现能燃烧。乙同学实验中“溶液慢慢浑浊且变红”的原因请用化学方程式表示:___________________。
(四)丙同学在做实验时,不小心将镁条掉入到碳酸氢钠溶液中,发现产生大量的气泡和白色不溶物。他非常好奇,进行了如下探究。
【提出问题】镁条与碳酸氢钠溶液反应,产生的气体和白色不溶物分别是什么?
【查阅资料】
Mg(OH)2 | MgCO3 | |
溶解性 | 难溶于水 | 微溶于水 |
热稳定性 | 受热易分解,能生成两种氧化物 | 受热易分解,能生成两种氧化物 |
实验探究一:镁条与碳酸氢钠溶液反应产生什么气体呢?
猜想 | 实验方法 | 现象 | 结论 | |
① | 二氧化碳 | 收集气体于集气瓶中,而后将气体通入澄清石灰水中; | 无明显现象 | 猜想①不成立 |
② | 氧气 | 收集气体于集气瓶中,而后将________放入瓶中; | 无明显现象 | 猜想②不成立 |
③ | 氢气 | 第一步,点燃产生的气体; 第二步,在火焰上罩内壁涂有石灰水的烧杯。 | 气体能被点燃; 烧杯内壁无现象; | 猜想______成立 (填序号) |
④ | _____ | |||
⑤ | 甲烷 | |||
实验探究二:
【提出问题】镁条与碳酸氢钠溶液反应,产生的白色不溶物是什么?
【作出猜想】丙同学根据资料分析认为白色不溶物可能是Mg(OH)2和MgCO3中的一种或两种。
【进行实验】
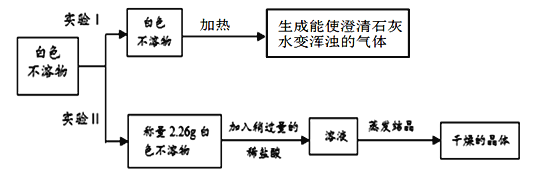
(1)根据实验Ⅰ的现象,写出加热白色不溶物时一定发生的化学反应的方程式__________;
(2)实验Ⅱ中 称量“干燥的晶体”质量为2.85g,由此通过计算确定白色不溶物是成分是_________________。(请你写出计算过程)
【题目】实验室有一包固体药品,可能含有BaSO4、Na2CO3、CuSO4、NaCl、CaCl2、NaOH中的一种或几种,为确定其成分,某班同学在老师的指导下进行探究。
(一)定性探究:
Ⅰ.称取少量样品,加入足量水中充分溶解,过滤后得到白色沉淀和无色滤液。由实验现象可知,原固体中一定不含____;
Ⅱ.取Ⅰ中得到的滤液少量,设计实验继续探究原固体的成分,请帮他们完成实验报告并回答问题。
操作 | 现象 | 结论 |
向滤液中加入足量氯化钙溶液 | 产生白色沉淀 | 原固体中一定含有____ |
取上层清液,滴加____ | ____ | 原固体中不含NaOH |
其中,步骤加入足量氯化钙溶液的目的除了检验一定含有的物质外,还能起到的作用是____;
Ⅲ.再取Ⅰ中得到的滤液少量,进行如下操作:
![]()
同学们认为:原固体中一定含有NaCl。但是老师指出这个结论不正确,其理由是___(填序号)
A.滤液中含有Na2CO3,也能和AgNO3反应生成沉淀
B.滤液中的NaCl可能是由原固体中的Na2CO3和CaCl2反应生成
(二)定量探究:
在老师的指导下同学们又精确称量了10g原固体,进行如下实验:
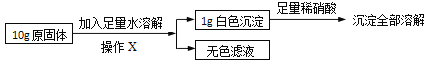
同学们认为,根据“沉淀全部溶解”的现象可确定白色沉淀的成分是____,则原固体中一定不含____;其中,操作X的名称是____,无色滤液中一定含有的阳离子是____。
试根据生成沉淀的质量计算原固体中氯化钙的质量分数,写出计算过程_____。