题目内容
【题目】水是生命之源!“珍惜水、节约水、爱护水”是每个公民应尽的义务和责任。
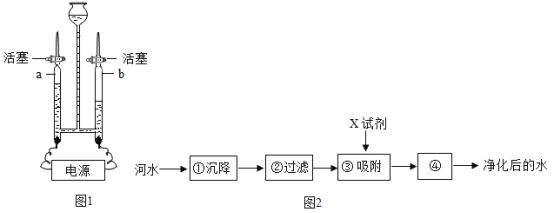
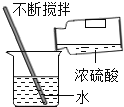
(1)用如图1所示装置进行电解水的实验,a、b两玻璃管中收集到的气体质量比为_____,反应的化学方程式为_____,该实验证明水是由_____组成的;
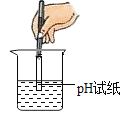
(2)饮用硬度过大的水不利于人体健康,在生活中可用_____区分硬水和软水;
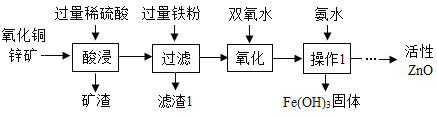
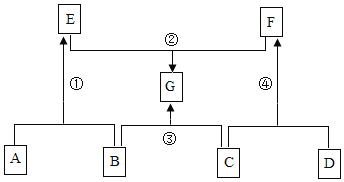
(3)如图2是自来水厂净化水的主要步骤。有关说法错误的是_____(填字母);
A 步骤①中可加入明矾作絮凝剂
B X试剂可以是活性炭
C 步骤④的作用是消毒杀菌
D 净化后的水为纯净物
(4)下列做法会造成水体污染的是_____(填序号)。
①工业废水处理达标后排放
②随意丢弃废旧电池
③提倡使用无磷洗衣粉
④合理使用化肥和农药
(5)现有6.4g某种铁的氧化物,用足量的CO将其完全反应,将生成的气体通过足量澄清石灰水,得到沉淀10.0g,则这种铁的氧化物可能是_____。
A FeO
B Fe2O3和Fe3O4
C FeO和Fe3O4
D Fe3O4
【答案】8:1 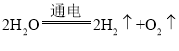 氢元素和氧元素 肥皂水 D ② C
氢元素和氧元素 肥皂水 D ② C
【解析】
(1)a、b两玻璃管中收集到的气体质量比为8:1,反应的化学反应方程式为: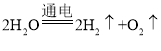 ;该实验证明水是由氢元素、氧元素组成的;
;该实验证明水是由氢元素、氧元素组成的;
(2)在生活中可用肥皂水区分硬水和软水,向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水;
(3)A.步骤①中可加入明矾作絮凝剂,该选项说法正确;
B.X试剂可以是活性炭,因为活性炭能够色素、异味等,该选项说法正确;
C.步骤④的作用是消毒杀菌,该选项说法正确;
D.净化后的水中仍然含有溶于水的物质,是混合物,该选项说法不正确;
(4)工业废水处理达标后排放、提倡使用无磷洗衣粉、合理使用化肥和农药,均有利于防治水体污染;随意丢弃废旧电池,会污染水体和土壤;
(5)设二氧化碳质量为x,
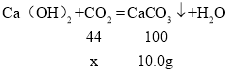
![]()
x=4.4g,
4.4g二氧化碳中氧元素质量为:4.4g×![]() ×100%=3.2g,
×100%=3.2g,
氧化亚铁、氧化铁、四氧化三铁和一氧化碳反应的化学方程式为:
FeO+CO![]() Fe+CO2,Fe2O3+3CO
Fe+CO2,Fe2O3+3CO![]() 2Fe+3CO2,Fe3O4+4CO
2Fe+3CO2,Fe3O4+4CO![]() 3Fe+4CO2,
3Fe+4CO2,
由反应的化学方程式可知,反应生成的二氧化碳中的氧元素一半来自于一氧化碳,一半来自于铁的氧化物,因此铁的氧化物中氧元素质量为:![]() =1.6g,
=1.6g,
6.4g某种铁的氧化物中氧元素质量分数为:![]() ×100%=25%,
×100%=25%,
氧化亚铁、氧化铁、四氧化三铁中氧元素质量分数分别是:![]() ×100%=22.2%,
×100%=22.2%,![]() ×100%=30%,
×100%=30%,![]() ×100%=27.6%,由以上计算可知,这种铁的氧化物不可能是氧化亚铁、Fe2O3与Fe3O4的混合物、Fe3O4,可能是FeO与Fe3O4的混合物,故选C。
×100%=27.6%,由以上计算可知,这种铁的氧化物不可能是氧化亚铁、Fe2O3与Fe3O4的混合物、Fe3O4,可能是FeO与Fe3O4的混合物,故选C。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是
A.表中a的值为5.6 B.X可能是该反应的催化剂
C.X可能含有氢元素 D.X只含碳元素