题目内容
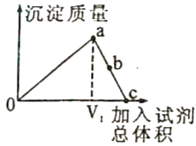
【题目】取大理石和稀盐酸反应后的废液50g,向其中逐滴加入碳酸钠溶液,根据实验测得的数据绘出如图所示的曲线图,其中纵坐标m是实验得到的沉淀或气体的质量,横坐标表示的是碳酸钠溶液的质量。
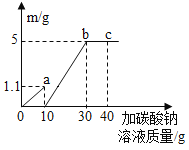
(1)当滴加20g碳酸钠溶液时,所得溶液中的溶质是 (填化学式)。
(2)当滴加30g碳酸钠溶液时,所得溶液中氯化钠的质量分数是多少?
【答案】(1) NaCl、CaCl2 ;(2) 11.9%
【解析】
(1)由图可知,取大理石和稀盐酸反应后的废液50g,向其中逐滴加入碳酸钠溶液,先产生气体,后产生沉淀。说明大理石和稀盐酸反应后的50g废液中含有稀盐酸及稀盐酸与碳酸钙反应生成的氯化钙。当滴加20g碳酸钠溶液时,由图可知,稀盐酸反应完,氯化钙反应一部分,故所得溶液中的溶质是稀盐酸与碳酸钠反应生成的氯化钠及未反应完的氯化钙,其化学式为:NaCl、CaCl2;
(2)设生成1.1g二氧化碳时,生成氯化钠的质量为x。

![]()
x=2.925g
设生成5g碳酸钙时,生成氯化钠的质量为y。
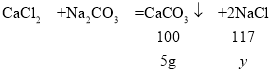
![]()
y=5.85g
当滴加30g碳酸钠溶液时,所得溶液中氯化钠的质量分数是:![]() ×100%≈11.9%
×100%≈11.9%
答:当滴加30g碳酸钠溶液时,所得溶液中氯化钠的质量分数是11.9%。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目