题目内容
【题目】(5分)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)氯化钠、铁、过氧化氢三种物质中,由离子构成的是 (填写化学式)。
(2)A、B、C、D表示四种物质,在高温条件下,A和B反应生成C和D,微观示意图如下所示。
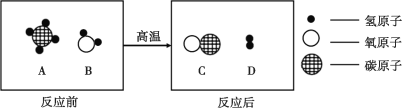
①反应后,生成C和D两种粒子的个数比为 。
②若有3 g D生成,参与反应的A质量为______g。
③下列结论中,正确的是_______。
a.B和C属于氧化物
b.反应前后各元素化合价均发生改变
c.反应前后分子的个数没有改变
d.A物质中氢元素的质量分数为25%
【答案】(1)![]() ;(2)①1:3;②8;③a、d.
;(2)①1:3;②8;③a、d.
【解析】(1)构成物质的微粒有分子、原子和离子,氯化钠、铁、过氧化氢三种物质中铁由原子构成过氧化氢由分子构成,而氯化钠则由钠离子和氯离子构成;
(2)根据图示的分子结构可知该反应的方程式为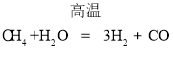 ;
;
①由方程式可以看出生成C和D两种粒子的个数比为1:3;
②若有3g D生成,设参与反应的A质量为x,
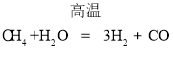
16 6
x 3g
![]() x=8g
x=8g
③a. B和C分别是水和一氧化碳,所以两者属于氧化物,a正确;b.根据方程式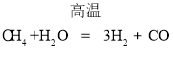 中反应前后的物质情况可知碳、氢元素的化合价均发生了改变,但是氧元素的化合价没有变化,b错误;c.根据方程式
中反应前后的物质情况可知碳、氢元素的化合价均发生了改变,但是氧元素的化合价没有变化,b错误;c.根据方程式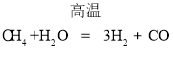 中反应前后的分子个数情况可知分子个数发生了改变,c错误;d、A是
中反应前后的分子个数情况可知分子个数发生了改变,c错误;d、A是![]() ,其中氢元素的质量分数为
,其中氢元素的质量分数为![]() ×100%=25%,d正确;
×100%=25%,d正确;
试题分析:(1)根据由离子构成的物质一般是含金属离子或铵根离子的化合物可知,氯化钠是由离子构成;
(2)根据微观模型图分析每个分子的构成可知,该反应是甲烷和水反应生成一氧化碳和氢气,根据质量守恒定律书写其反应方程式,可推断C、D的粒子个数比;根据方程式中参加反应的甲烷和生成氢气的质量比计算生成3g氢气时甲烷的质量;根据B和C分别是水和一氧化碳,所以都属于氧化物分析;根据方程式分析碳、氢元素的化合价均发生改变,氧元素的化合价没有变化,反应前后的分子个数发生改变分析;根据A是甲烷,计算甲烷中氢元素的质量分数分析.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】(6分)人类生存离不开能源。
(1)南京家用燃料的更新过程如下:

①煤、液化石油气、管道煤气均属于 (填“混合物”或“纯净物”)。
②下列有关家用燃料更新的理由,不正确的是_____(填字母序号)。
A.天然气属可再生能源
B.气体燃料比固体燃料利用率更高
C.减少煤燃烧过程中产生的污染物
D.气体燃料便于管道输送
③相同条件下,气体体积比等于分子数比。现有一套以液化石油气(主要成分为C4H10)为燃料的灶具,若要改为以天然气为燃料的灶具,应采取的措施是
A.燃料气和空气的进入量都减小
B.燃料气和空气的进入量都增大
C.增大燃料气进入量或减小空气进入量
D.减小燃料气进入量或增大空气进入量
(2)乙醇(C2H5OH)是一种绿色燃料。将一定量的乙醇和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:下列判断不正确的是
物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.6 | 8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
A.表中a的值为2.8
B.X可能是这个反应中的催化剂
C.X可能含有氢元素
D.若起始时氧气的质量是9.6g,则无X生成