题目内容
【题目】燃烧是人类最早利用的化学反应之一,但它却是一把双刃剑。
(1)据报道,江苏响水县某化工厂发生的特大爆炸事故,是由于硝化废料处理不当,发生级慢氧化引发自燃导致的。请从燃烧条件的角度分析,缓慢氧化引发自燃现象的原因: __________。大火无情,重在防范。在生活中,能有效预防火灾的措施有____________。(填序号,下同)
①不乱拉乱接电线、电源电器 ②建立定期防火检查,更换灭火器药剂
③控制、隔离易燃物 ④家庭装修不用或少用易燃材料
(2)可燃物在有限的空间里极速燃烧可导致爆炸,下列混合物遇明火不会发生爆炸的是__________。
a煤气和空气 b N2 和 O2 c面粉和 O2 d H2 和 CO
(3)请根据燃烧的条件或灭火的原理解释以下成语的化学含义。
①煽风点火:_____________。
②釜底抽薪:_____________。
(4)在点燃的条件下,某反应的微观示意图如下图所示,请把图中 A、B 框中的微观粒子补画齐全___________。该反应属于_________反应。(填基本反应类型)
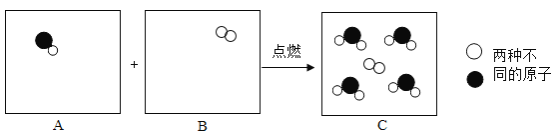
【答案】可燃物内部由于缓慢氧化产生的热量累积起来,温度升高达到可燃物的着火点 ①②③④ bd 氧气充足时,物质燃烧更旺 使得炉内没有了可燃物,即可燃物与炉内助燃物分离,导致“釜”下之火熄灭 图A中补充3个![]() ,图B中补充3个
,图B中补充3个![]() 化合反应
化合反应
【解析】
(1)可燃物内部由于缓慢氧化产生的热量累积起来,温度升高达到可燃物的着火点,从而引起自燃;大火无情,重在防范,在生活中:
①不乱拉乱接电线、电源电器,能有效预防火灾;
②建立定期防火检查,更换灭火器药剂,能有效预防火灾;
③控制、隔离易燃物,能有效预防火灾;
④家庭装修不用或少用易燃材料,能有效预防火灾;故选:①②③④;
(2)煤气、面粉都具有可燃性,跟氧气混合后遇到明火会发生爆炸;N2不能燃烧,跟氧气混合后遇到明火不会发生爆炸;H2和CO都具有可燃性,但未跟氧气混合,遇到明火不会发生爆炸,故选:bd;
(3)①煽风点火:比喻煽动别人闹事,根据燃烧的条件或灭火的原理可知,氧气充足时,物质燃烧更旺;
②釜底抽薪:使得炉内没有了可燃物,即可燃物与炉内助燃物分离,导致“釜”下之火熄灭;
(4)根据反应前后原子的种类数目数目不变,在图A中应补充3个![]() ,图B中应补充3个
,图B中应补充3个![]() ;此反应是两种物质反应生成一种物质的反应,属于化合反应。
;此反应是两种物质反应生成一种物质的反应,属于化合反应。

【题目】某化学实验小组对 “影响石灰石与盐酸反应速率的因素——盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与。
[进行实验]室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去)。
(1)石灰石与盐酸反应的化学方程式为___________________。
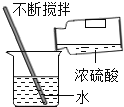
(2)按如图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是____。
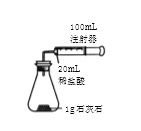
开始实验时,应将20mL稀盐酸_____________(填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中。
[处理数据](3)实验小组进行实验后,获得的相关实验数据如表所示:
实验 编号 | 盐酸的溶质质量分数 (均取20mL) | 石灰石固体形状 (均取1g) | 二氧化碳的体积/mL (均收集前30s的气体) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
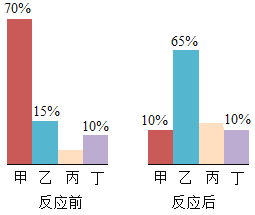
①要比较不同溶质质量分数的盐酸对反应速率的影响,可选择的实验编号是_______(写一组),由此可得到的结论是_______________。
②从上述实验得出石灰石的颗粒大小对反应速率影响的结论是_____________。
(4)如表是实验时记录生成的二氧化碳气体的体积和对应的时间的一组实验数据(每间隔4s读数一次):
时间/s | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 | |
气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20s后反应速率逐渐变____,其主要原因是___。
(5)你认为影响石灰石与盐酸反应速率的因素还有____,请设计实验方案验证你的猜想:____
【题目】请回忆你和老师共同学习的酸和碱反应的实验探究,并按要求进行实验设计与
(实验探究)
(1)据图设计酸和碱反应:
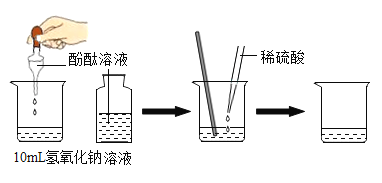
实验步骤 | 实验现象 | 结论 |
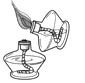
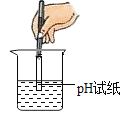
①向烧杯中加入 10mL 氢氧化钠溶液,并滴入几滴酚酞试液 | ①溶液颜色_____; | 酸和碱发生了中和反应。 |
②再用滴管慢慢滴入稀硫酸,并不断搅拌溶液 | ②不断搅拌溶液至溶液颜色变成_____色 |
写出硫酸与氢氧化钠反应的化学方程式__________________。
(2)为探究上述酸、碱反应后硫酸是否过量,甲、乙两位同学设计了以下方案:
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
甲同学的方案 | 取样,滴入几滴无色酚酞溶液 | 酚酞溶液不变色 | 酸、碱恰好完全反应 |
乙同学的方案 | 取样,滴入几滴紫色石蕊溶液 | 溶液变红 | 硫酸过量 |
(实验评价)
①甲、乙两位同学设计的二个方案中,有一个正确的方案,是________(填“甲”“乙” )。
②请分析另一个同学方案错误的原因是__________。
(实验反思)
探究硫酸和氢氧化钠反应后硫酸是否有剩余,还可选择一种试剂是(__________)
AFe BCa(OH)2 CCuO DNa2CO3