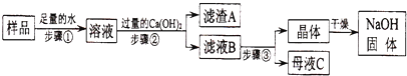
��Ŀ����
����Ŀ����һ�������ϵ��й�֪ʶ
��1������ʹ�ý����Ⱥ����ˡ���ͭ������������ʱ�����������ſ�ʼ����ʹ�������ϣ���Ҳ��ӳ��Cu��Fe��Al���ֽ����Ļ����ǿ������˳����_____��
��2��������ʱ�ھ��С����������Ϊͭ��֮˵���û�ѧ����ʽ��ʾ��ԭ��_____��
��3������¶���ڿ����������⣬д��һ�ַ�ֹ��������ķ���_____��
������ͬѧ������ijɷ֡������Ʋ����������弰�������������ȷֽ���о���
�����������������Ʋ����������壨FeC2O4��nH2O��
���ϣ���FeSO4����������������ת��ΪFe2(SO4)3��
��FeSO4���ܽ�����±���
�¶�/�� | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
�ܽ��/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
���Ʊ����̣�
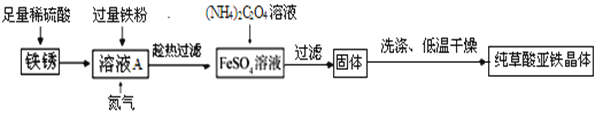
��1����Һ����������ۣ������ķ�Ӧ�У�Fe+Fe2(SO4)3=3FeSO4��_____����ַ�Ӧ��Ҫ���ȹ��˵�Ŀ����_____��
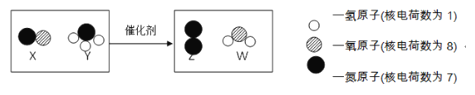
��2�������в��������������巴Ӧ�Ļ�ѧ����ʽΪ_____��
��3���Ʊ������У���Һ��ͨ�뵪����������_____��
������̽��FeC2O4��nH2O�ȷֽ�IJ��Pn��ֵ
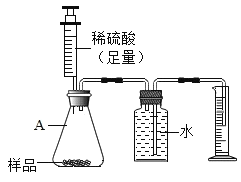
��ʵ��װ�ã�
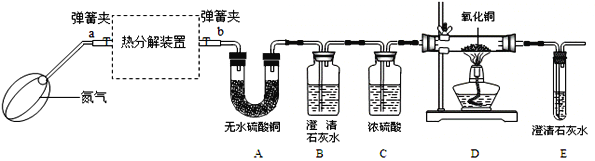
����:��FeC2O4��nH2OΪ����ɫ��ĩ��FeO��Fe3O4���Ǻ�ɫ���壬����FeO�ױ�����������
��FeC2O4��nH2O������300����ȫʧȥ�ᾧˮ������������400����ʣ��������ȷֽ������ɫ���塢CO2��CO��
��ʵ�������
��1����ͨ��Eװ���г���ʯ��ˮ�������֤���������������ȷֽ����CO��������B��Cװ��֮������ʢ��_____�����Լ����ƣ���ϴ��ƿ��
��2���ȹ��뵪�����ټ��ȷֽ�װ�õ�ԭ����_____��
��3��ָ������ʵ��װ�ò���֮��_____��
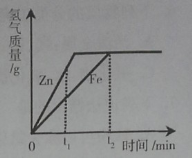
��4��ȡ3.60gFeC2O4��nH2O��������ʵ�鲽�����ʵ�飬����ȷֽ�װ���й����������¶ȱ仯��������ͼ��ʾ��
��FeC2O4��nH2O��n��ֵΪ_____��
�ڷ�Ӧ���ȷֽ�װ���в����ĺ�ɫ����Ϊ_____���ѧʽ����
�۲��������������ȷֽ�ķ���ʽΪ_____��
������ͼ��1.44g�����ڿ����г�ּ��ȣ���������0.16g���˹���(����������)Ϊ_____��
���𰸡�Al��Fe��Cu Fe+CuSO4====Cu+FeSO4 ˢ�ᡢͿ�͵� Fe+H2SO4=FeSO4+H2�� ��ֹFeSO4��ᾧ�������ʧ (NH4)2C2O4+FeSO4=FeC2O4��+(NH4)2SO4
��nH2O+(NH4)2C2O4+FeSO4=FeC2O4.��nH2O��+(NH4)2SO4 ��ֹFeSO4������Fe2(SO4)3 ����������Һ �ų�װ����ԭ�����壬��ֹ��������(�����𰸾��ɣ� û�н���β������ 2 FeO FeC2O42H2O![]() FeO+CO��+CO2��+2H2O Fe2O3
FeO+CO��+CO2��+2H2O Fe2O3
��������
��һ����1������ʹ�ý���Խ�磬˵���ý���Խ�����ã�������ֽ����Ļ����ǿ������˳����Al��Fe��Cu��
��2��������ʱ�ھ��С����������Ϊͭ��֮˵����ԭ������������ͭ��Ӧ��������������ͭ����Ӧ�Ļ�ѧ����ʽΪ��Fe+CuSO4�TCu+FeSO4��
��3������¶���ڿ����������⣬ˢ�ᡢͿ�͵ȿ��Է�ֹ�������⣻
��������1����Һ����������ۣ�������������Ӧ�������������������ᷴӦ����������������������Ӧ�Ļ�ѧ����ʽΪ��Fe+Fe2��SO4��3��3FeSO4��Fe+H2SO4�TFeSO4+H2������ַ�Ӧ��Ҫ���ȹ��˵�Ŀ���ǣ���ֹFeSO4��ᾧ�������ʧ��
��2�������в��������������巴Ӧ�Ļ�ѧ����ʽΪ��(NH4)2C2O4+FeSO4=FeC2O4��+(NH4)2SO4��NH4��2C2O4+FeSO4+nH2O��FeC2O4nH2O��+��NH4��2SO4��
��3���Ʊ������У���Һ��ͨ�뵪���������Ƿ�ֹFeSO4������Fe2��SO4��3��
��������1����ͨ��Eװ���г���ʯ��ˮ�������֤���������������ȷֽ������CO��������C��Dװ��֮������ʢ������������Һ��ϴ��ƿ�������ն�����̼���壻
��2���ȹ��뵪�����ټ��ȷֽ�װ�õ�ԭ���ǣ��ų�װ����ԭ�����壬��ֹ�������ţ�
��3������ʵ��װ�ò���֮���ǣ�û�н���β���������ᵼ��һ����̼��ɢ����������Ⱦ������
��4���ٽᾧˮ����Ϊ��3.60g��2.88g��0.72g
����������144��18n��2.88g��0.72g
n��2
��3.60g��������Ԫ������Ϊ��3.60g��![]() ��1.12g
��1.12g
��Ӧ���ȷֽ�װ���в����ĺ�ɫ��������ԭ�Ӻ���ԭ�Ӹ�����Ϊ![]() ��
��![]() ��1��1�����ȷֽ�װ���в����ĺ�ɫ������������������ѧʽΪ��FeO��
��1��1�����ȷֽ�װ���в����ĺ�ɫ������������������ѧʽΪ��FeO��
�۲��������������ȷֽ���������������������̼��һ����̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��FeC2O42H2O![]() FeO+CO��+CO2��+2H2O��
FeO+CO��+CO2��+2H2O��
������ͼ��1.44g�����ڿ����г�ּ��ȣ���������0.16g��˵���μӷ�Ӧ����������Ϊ0.16g��
�˹��壨�������������ԭ�Ӻ���ԭ�Ӹ�����Ϊ![]() ��
��![]() ��2��3����������������������������
��2��3����������������������������

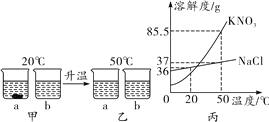
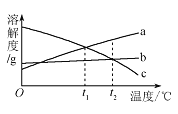
����Ŀ����ͼ��ʾ���ڷֱ�ʢ�� 100g ˮ���ձ��з��� KNO3 ����ܽ⣬��˵����ȷ����
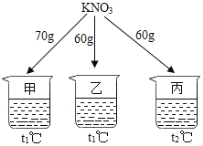
�¶ȣ����� | t1 | t2 |
KNO3���ܽ�ȣ�g/100g ˮ�� | 60 | 90 |
A. �ס��һ�Ϻ�Ϊt1��IJ�������Һ
B. ��������t2�棬��Һ��������
C. �ҡ�����Һ�������������
D. ��������t1�棬�о�������