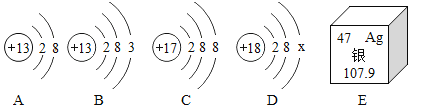
��Ŀ����
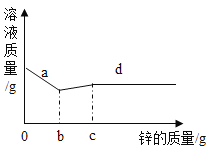
����Ŀ����ͼ1��С����20��ʱ���е�ϵ��ʵ��ʾ��ͼ����-�ݱ�ʾʵ��������Һ��ͼ2��NaCl��KNO3���ܽ�����ߣ�
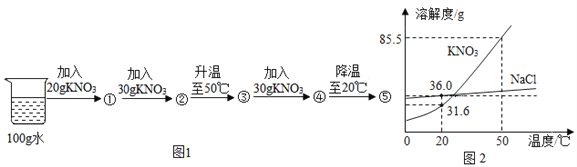
��1��20��ʱ��KNO3���ܽ�ȣ�S��=________������ _______������͡������͡�����Һ��
��2��50��ʱ������NaCl��Һ�����ʵ�����������w1���뱥��KNO3��Һ�����ʵ�����������w2���Ĵ�С��ϵ�ǣ�w1______w2���������=����������
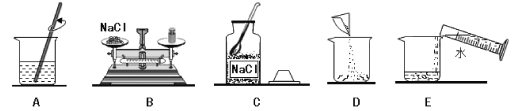
��3��С�����֣�������50�棬�ڡ��۵Ĺ�����������ˮ����������������ȷ����______������ţ�
a���١��ھ�Ϊ��������Һ
b���ڡ��۵Ĺ��������������������
c���ܡ��ݵĹ���������KNO3����53.9g
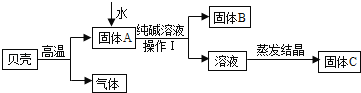
��4����ȥKNO3�����л��е�����NaCl��ʵ�����Ϊ��������ˮ�ܽ�����ȵõ��ȱ�����Һ��____�����ˡ�ϴ�ӡ������KNO3��
���𰸡� 31.6g�� ���� �� b ���½ᾧ
��������������ѧ֪ʶ��������Ϣ֪����1��20��ʱ��KNO3���ܽ�ȣ�S��= 31.6g�����DZ�����Һ��100gˮ�м�������ء�20g��30g��30g��80g����2��50��ʱ���Ȼ����ܽ��С��������ܽ�ȣ�����NaCl��Һ�����ʵ�����������w1���뱥��KNO3��Һ�����ʵ�����������w2���Ĵ�С��ϵ�ǣ�w1��w2����3��������50�棬�ڡ��۵Ĺ�����������ˮ������a����Ϊ��������Һ����Ϊ������Һ��20��ʱ������ܽ����31.6g����a����b���ڡ��۵Ĺ��������������������50��ʱ������ܽ����85.5g��20��ʱ������ܽ����31.6g����b��ȷ��c��20��ʱ������ܽ����31.6g���ܡ��ݵĹ���������KNO3�����ǡ�20g��30g��30g ��31.6g��48.4g����c����4����ȥKNO3�����л��е�����NaCl��ʵ�����Ϊ��������ˮ�ܽ�����ȵõ��ȱ�����Һ�����½ᾧ�����ˡ�ϴ�ӡ������KNO3��������ܽ�����¶�Ӱ��仯�ϴ��Ȼ����ܽ�����¶�Ӱ��仯����
�㾦��������Һ�Ͳ�������Һ��һ�������¿����ת����������Һ����������������![]() ��100����
��100����

 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д� â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�