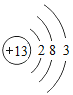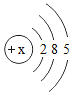题目内容
【题目】有三组固体混合物:
①Na![]() O
O![]() (过氧化钠)和NaOH的混合物,其中Na的质量分数是58% ;
(过氧化钠)和NaOH的混合物,其中Na的质量分数是58% ;
②FeSO![]() 和Fe
和Fe![]() (SO
(SO![]() )
)![]() 的混合物,其中Fe的质量分数是31%;
的混合物,其中Fe的质量分数是31%;
③Na![]() S Na
S Na![]() SO
SO![]() ,和Na
,和Na![]() SO
SO![]() 的混合物,其中S的质量分数是25.6%。
的混合物,其中S的质量分数是25.6%。
其中含氧元素的质量分数最高的一组是___为__%
【答案】② 46
【解析】
①Na2O2(过氧化钠)、NaOH的混合物中钠原子与氧原子个数比为1:1,所以其中Na的质量分数是58%时,O的质量分数为58%×![]() ≈40%;
≈40%;
②FeSO4和Fe2(SO4)3的混合物,其中Fe的质量分数是31%,则混合物硫酸根的质量分数为1-31%=69%,因此混合物中O的质量分数为69%×![]() =46%;
=46%;
③Na2S、Na2SO3和Na2SO4的混合物中钠原子与硫原子的个数比为2:1,所以其中S的质量分数是25.6%时,Na的质量分数为25.6%×![]() =36.8%,则固体混合物中含氧元素的质量分数=1-25.6%-36.8%=37.6%。
=36.8%,则固体混合物中含氧元素的质量分数=1-25.6%-36.8%=37.6%。

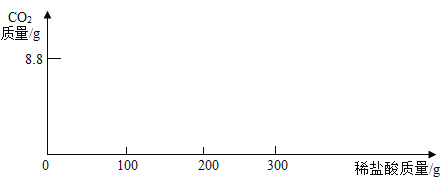
【题目】某研究性学习小组称取含NaCl的Na2CO3固体25 g,将其配制成溶液,再向其中逐滴加入足量的7.3%的稀盐酸,使气体完全放出,共收集到 8.8 g CO2气体。
(1)计算原固体中Na2CO3的质量分数____________和消耗稀盐酸的总质量____________(写出计算过程)。
(2)下表为研究性学习小组向上述配制的混合液中分三次逐滴加入(边加边振荡)稀盐酸后所记录的部分数据。经查阅资料知Na2CO3与HCl反应可以分两步进行:Na2CO3+HCl=NaCl+NaHCO3,NaHCO3+HCl=NaCl+H2O+CO2↑。
①请完成表格中未填的部分。
实验次数 | 每次产生的CO2的质量/g |
第一次先逐滴滴加稀盐酸100 g | ________ |
第二次再逐滴滴加稀盐酸100 g | 8.8 |
第三次再逐滴滴加稀盐酸100 g | 0 |
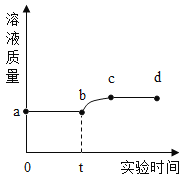
②根据表中数据在坐标系中画出CO2的质量(纵坐标)与所加入稀盐酸的质量(横坐标)的关系图________。
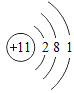
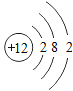
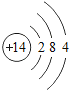
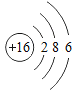
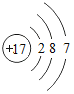
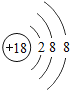
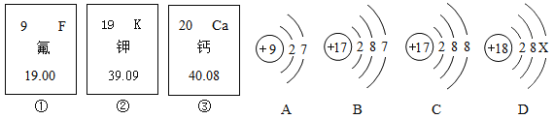
【题目】下表为元素周期表中某一周期元素的原子结构示意图.请回答下列问题:
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
(1)表中磷原子的核电荷数x=____.
(2)在化学反应中,每个铝原子失去____个电子形成铝离子.
(3)镁元素与氯元素形成的化合物的化学式为____
(4)上述元素在周期表中处于同一周期的原因是它们原子的____相同.