题目内容
【题目】(4分)某化学兴趣小组对一包含有铜、银、锰的混合金属粉末进行了分离,获得了一种金属和一种盐的晶体。他们将三种金属随意编号为A、B、C,并设计了如下流程:
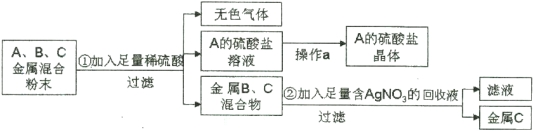
(1)金属B是 (填元素符号),操作a的名称是 。
(2)已知A的硫酸盐中A元素显+2价,请写出①、②反应的化学方程式:
① ;
② ;
【答案】(1)Cu 蒸发结晶
(2)①Mn+H2SO4==MnSO4+H2↑
②Cu+2AgNO3==Cu(NO3)2+2Ag
【解析】
试题分析:(1)由金属活动性顺序的应用:位于氢前面的金属能酸中的氢置换出来生成氢气,由于铜和银均位于氢的后面,根据反应流程,三种金属的混合物中加入硫酸生成了氢气,那么说明锰位于氢的前面,故A是金属锰;铜位于银的前面,能把硝酸银中的银置换出来,故最终得到的金属C是银,那么B是铜;操作a,物质由溶液变成了晶体,故操作a是蒸发;
(2)锰与硫酸反应生成的是硫酸锰和氢气:Mn+H2SO4==MnSO4+H2↑;
铜和硝酸银反应生成的是银和硝酸铜:Cu+2AgNO3==Cu(NO3)2+2Ag 。

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目