题目内容
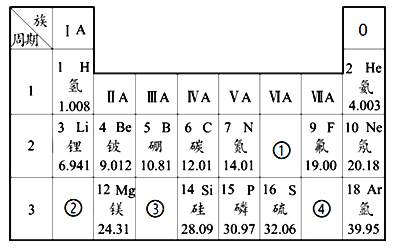
【题目】下表是元素周期表中第2、3周期的元素,请回答有关问题。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(1)下列各组具有相似化学性质的元素是_____(填字母序号);
A Na、Cl B O、S C F、Cl D Cl、Ar
(2)写出一条第三周期元素原子的核外电子排布规律_____;
(3)笫8号元素与笫13号元素的原子形成化合物的化学式为_____;在该化合物中13号元素的化合价为_____;
(4)某粒子的结构示意图为 ,在化学变化中易失2个电子,该粒子的符号为_____。
,在化学变化中易失2个电子,该粒子的符号为_____。
【答案】BC 同一周期的元素的原子,核外电子层数相同(合理即可) Al2O3 +3 Mg
【解析】
(1)A.Na、Cl的最外层电子数不同,不具有相似的化学性质;
B.O、S的最外层电子数相同,具有相似的化学性质;
C.F、Cl的最外层电子数相同,具有相似的化学性质;
D.Cl、Ar的最外层电子数不同,不具有相似的化学性质;
故填:BC。
(2)第三周期元素原子的核外电子层数相同,均为三层;
故填:同一周期的元素的原子,核外电子层数相同。
(3)8号元素是氧元素,13号元素是铝元素,在化合物中,铝元素显+3价,氧元素显-2价,所以二者组成的化合物的化学式为![]() ,铝元素为+3价。
,铝元素为+3价。
(4)某粒子的结构示意图为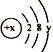 ,在化学变化中易失2个电子,则最外层电子数y=2,故x=2+8+2=12,该粒子为镁原子,符号为
,在化学变化中易失2个电子,则最外层电子数y=2,故x=2+8+2=12,该粒子为镁原子,符号为![]() 。
。

 应用题作业本系列答案
应用题作业本系列答案