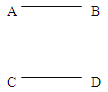��Ŀ����
����Ŀ����13�֣�A��B��C�ֱ���Zn��Cu��Ag���ֽ����е�һ�֡�Ϊ�˴����ǵĻ�����з���
������A�������B��C���Σ���������ʵ�������
��ش��������⣺
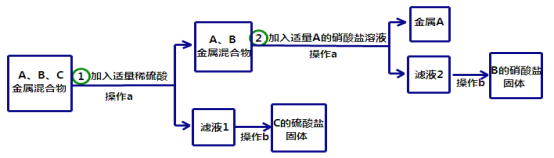
д���������з�����Ӧ�Ļ�ѧ����ʽ ��
A��B��C���ֽ����Ļ��˳���� > > ��
����b����Ҫ�õ��������������� ��
����A�� ���ѧʽ����ͬ����B���������� ��
��13�˵�пͶ�뵽98��ϡ������ǡ����ȫ��Ӧ�������ɵ������������Ƕ��٣�![]()
���𰸡���1��Zn + H2SO4 = ZnSO4 + H2�� ��2�� C��B��A ��3�� ��ֹҺ��ֲ����ȶ��ɽ�
��4��Ag Cu(NO3)2 ��5��0��4g
��������
�����������1�����ݽ����Ļ��˳�����ֽ���Zn��Cu��Ag��ֻ��п����ϡ���ᷴӦ�����Բ������з�����Ӧ�Ļ�ѧ����ʽ��Zn + H2SO4 = ZnSO4 + H2�����Ӷ������жϽ���CΪп
��2�����ݲ��������ڽ���Cu��Ag�������У�����A�������Σ�����û����˽���A�����Կ��ж�BΪͭ��A��ȻΪ������A��B��C���ֽ����Ļ��˳����C>B>A
��3������b�Ǵ���Һ�нᾧ�õ����壬��Ϊ�����������õ��������������ǣ����裬��ֹҺ��ֲ����ȶ��ɽ�
��4����������ķ�������AΪ������ѧʽΪ��Ag��B����������ͨ��ͭ����������Һ��Ӧ�õ�����Ϊ����ͭ����ѧʽΪ��Cu(NO3)2
��5�����ݻ�ѧ��Ӧ����ʽ��Zn + H2SO4 = ZnSO4 + H2����п��������������ϵ�������������������
�⣺������������Ϊx
Zn + H2SO4 = ZnSO4 + H2��
2
13g x
65:2=13g��x
X=0��4g