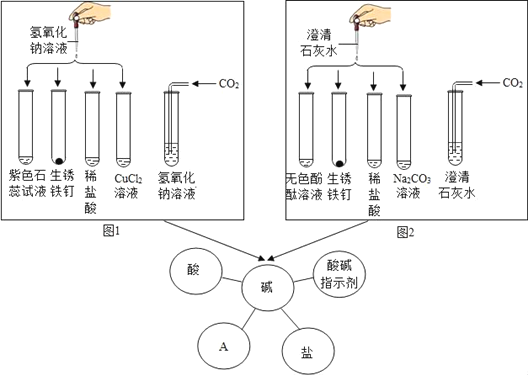
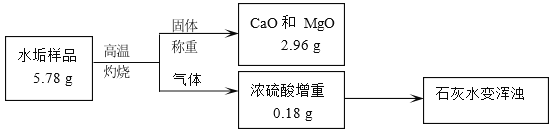
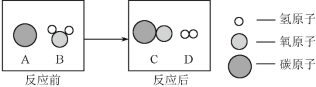
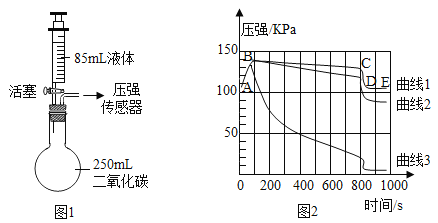
题目内容
【题目】水是生命之源,是人类最宝贵的资源,所以人们要有关心水、爱护水、节约水的意识。
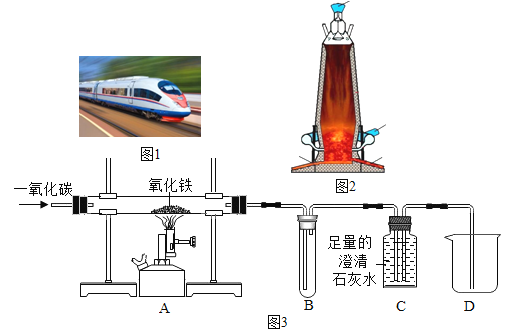
(1)如图是自来水厂净水过程示意图:
自来水厂生产自来水时,使用的净水方法有______。
A 沉淀 B 过滤 C 煮沸 D 蒸馏 E 吸附
(2)小红同学想检验自家的井水是硬水还是软水可以用______,在家中要把硬水转化为软水的最好方法是______。
(3)许多化学实验中都要用到水,在做铁丝燃烧的实验时,集气瓶中盛少量水的作用是______。
(4)“世界上最后一滴水就是人类的眼泪”。这句话警示我们要树立保护水资源的意识:一是节约用水,二是防止水体污染。请举一例节约用水的做法:______。
【答案】ABE 肥皂水 煮沸 防止生成物熔化溅落下来,使瓶底炸裂 洗衣水用来拖地后再冲厕所
【解析】
(1)根据自来水厂生产自来水时常用的净水方法进行分析判断。
(2)区分硬水和软水常用的方法是用肥皂水,根据日常生活软化硬水的方法进行解答。
(3)根据铁在氧气中燃烧的实验现象进行分析解答。
(4)根据节约用水的方法进行分析解答。
解:(1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附
(2)硬水和软水的区别在于所含的钙镁离子的多少,生活中可用肥皂水来区分硬水和软水,产生泡沫较多的是软水,较少的硬水。生活中常用煮沸或蒸馏的方法来降低水的硬度。
(3)在做铁丝燃烧的实验时,集气瓶中盛少量水是为了防止生成物熔化溅落下来,使瓶底炸裂。
(4)节约用水人人有责,如刷牙用口杯接水;工业用水重复利用;洗衣水用来拖地后再冲厕所;园林采用喷灌浇水;生活污水集中处理后再利用等。
故答案为:(1)ABE;(2)肥皂水;煮沸;(3)防止生成物熔化溅落下来,使瓶底炸裂;(4)刷牙用口杯接水;工业用水重复利用;洗衣水用来拖地后再冲厕所;园林采用喷灌浇水;生活污水集中处理后再利用等。

【题目】兴趣小组同学发现镁条在空气中久置表面会变黑,同学们对镁条变黑的条件及生成物进行了相关的探究。

(一)镁条变黑条件的探究
(查阅资料)常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
(猜想与假设)常温下,镁条变黑可能与O2、CO2、水蒸气有关。
(进行实验)通过控制与镁条接触的物质,利用如图装置(镁条长度为3cm,试管容积20mL),分别进行下列5个实验,并持续观察20天。
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mLNaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸再通入约4mLCO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水再通入约4mLCO2 | 镁条第3天开始变黑至20天全部变黑 |
(解释与结论)
(1)实验1和2中,NaOH浓溶液的作用是_____(用化学方程式表示)。
(2)实验3中,试管内的气体主要含有CO2、_____。
(3)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是_____(填编号)。
(4)根据上述实验,兴趣小组同学得出结论:镁条表面黑色物质的形成与_____有关。
(反思与评价)
(5)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是_____。
(二)对镁条变黑后生成物的探究
兴趣小组同学查阅资料,了解到镁条表面的黑色物质是一种混合物,其中主要成分碱式碳酸镁可表示为a Mg(OH)2·b MgCO3·c H2O。
(查阅资料)①Mg(OH)2、MgCO3受热易分解,各生成对应的两种氧化物;
②碱石灰是CaO和NaOH的固体混合物。
(进行实验)兴趣小组同学为进一步确定碱式碳酸镁组成,称取购买的碱式碳酸镁固体18.2g;装入硬质玻璃管,按如下图所示装置进行实验(假设装置A、C、D中所装药品均足量)。
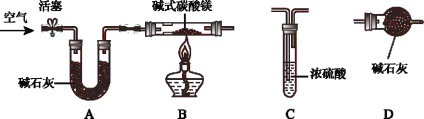
步骤一:连接A和B,打开活塞,通入空气;
步骤二:点燃酒精灯,依次连接装置A→B→_____→_____(填“C”,“D”);
步骤三:待装置B中固体完全反应后,停止加热,继续通入空气,直至冷却。反应前后称量相关装置和物质的总质量,其数据如下表:
反应前 | 反应后 | |
C:试管和所盛溶液 | 45.0g | 48.6g |
D:干燥管和固体 | 75.8g | 82.4g |
(解释与结论)
(1)“步骤三”中,当反应结束后,继续通入空气的目的是_____(写一条)。
(2)假设上述数据均准确,通过计算可得:该碱式碳酸镁中a:b:c=_____。
(3)有同学提出,在“步骤二”连接装置的最末端应再接一套装有碱石灰的装置,这样改进的目的是_____。