题目内容
【题目】实验室用块状大理石和5%的稀盐酸反应制取![]() ,观察不到气泡产生时,发现固体还有剩余,化学兴趣小组的同学对此进行探究(杂质不溶于水且不与酸反应)。
,观察不到气泡产生时,发现固体还有剩余,化学兴趣小组的同学对此进行探究(杂质不溶于水且不与酸反应)。
(提出问题)不再产生气泡的原因是什么?
(猜想假设)猜想一:盐酸已经完全反应
猜想二:剩余固体中无碳酸钙
猜想三:生成物或杂质附着在大理石表面,阻碍反应继续进行
(实验探究一)反应后溶液中是否有盐酸。
实验步骤 | 现象 | 结论 |
取上述反应后的清液,测溶液pH | 测得溶液 | 说明溶液显_____性,由此得出猜想一不成立的结论。 |
(质疑)有同学认为此结论不够严谨,还应考虑生成物对溶液酸碱性强弱的影响。
(补充实验)
①取干净的烧杯,另配制_____溶液,测得溶液![]() 。
。
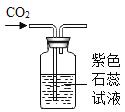
②取洁净的试管,加入适量水和紫色石蕊溶液,持续通入![]() ,发现溶液变为_____色。
,发现溶液变为_____色。
③另取洁净的试管,加入适量水,持续通入![]() 至饱和,测得溶液
至饱和,测得溶液![]() 。
。
以上三个补充实验中,能对质疑作出合理解释的是_____(填实验编号),由此可知,探究一种生成物不会使溶液的_____,猜想一不成立,反应后的溶液中有盐酸。
(实验探究二)剩余固体中是否有碳酸钙。
实验步骤 | 现象 | 结论 |
先振荡反应容器,使剩余固体和液体充分接触 | 仍无气泡产生 | 结论:假设_____不成立。 |
再向容器中滴加少量5%的稀盐酸 | 又有气泡产生,到不再产生气泡时,仍有固体剩余 |
综合探究实验一与探究实验二,可得出影响反应能否进行的因素之一是_____。
【答案】酸 氯化钙或![]() 红 ①③ 酸碱度受到影响 二 反应物的浓度大小
红 ①③ 酸碱度受到影响 二 反应物的浓度大小
【解析】
[实验探究一]由于溶液pH=3,所以溶液呈酸性;故填:酸。
[补充实验]①为了验证溶液的pH=3,不是由于生成的氯化钙造成的,取干净的烧杯,另配制氯化钙溶液,测得溶液pH=7;故填:氯化钙或![]()
②取洁净的试管,加入适量水和紫色石蕊溶液,持续通入CO2,发现溶液变为红色;故填:红。
以上三个补充实验中,能对质疑作出合理解释的是①和③;由此可知,探究一种生成物不会使溶液的酸碱度受到影响,猜想一不成立,反应后的溶液中有盐酸;故填:①③;酸碱度受到影响。
[实验探究二]
再向容器中滴加少量5%的稀盐酸,又有气泡产生。一段时间后,不再产生气泡,仍有固体剩余,可知仍然有碳酸钙固体剩余,可得出猜想二不成立。故填:二
综合探究实验一与探究实验二,可得出影响反应能否进行的因素之一是:反应物的浓度大小。故填:反应物的浓度大小。

【题目】课堂上,老师和同学们探究了二氧化碳的性质。请回答问题。
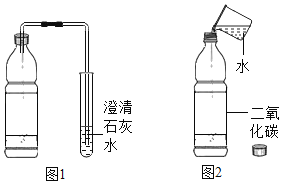
(学习情景)打开汽水瓶盖时,有气泡冒出。同学们将气体通入澄清石灰水中,石灰水变浑浊(如图),发生反应的化学方程式是_______________,实验后,老师要求同学们将试管中的浑浊物再次变得澄清,你认为可采用的方法是____________________。
(提出问题一)汽水中为什么会产生二氧化碳气体呢?
(作出猜想)汽水中溶有二氧化碳,二氧化碳能溶于水。
(进行实验)向一个收集满二氧化碳气体的质地较软的塑料瓶中加入![]() 体积的水、立即拧紧瓶盖,振荡,观察到的现象是_________________,得出二氧化碳能溶于水的洁论。
体积的水、立即拧紧瓶盖,振荡,观察到的现象是_________________,得出二氧化碳能溶于水的洁论。
(提出问题二)二氧化溶于水的过程中是否与水发生了化学反应?
(作出猜想)二氧化碳能与水发生化学反应,生成其它物质。
(实验方案)取三朵用紫色石蕊溶液染成紫色的干燥纸花,完成下列实验。
实验操作 | 实验现象及化学方程式 | 实验结论 |
步骤一:将第一朵纸花喷上稀醋酸 | 现象:紫色纸花变红 | 结论:二氧化碳能与水发生化学反应。化学方程式______________。 |
步骤二:将第二朵纸花直接放在盛滿二化碳的集气瓶中。 | 现象:紫色纸花没有变红 | |
步骤三:将第三朵纸花喷 上水后,再放入盛满二氧化碳的集气瓶中 | 现象: _________ | |
步骤四:将步骤三集气瓶 中的纸花取出,用吹风机烘干 | 现象: _________ | 结论: ________ |
(实验总结)汽水为混合物,至少含有以下三种物质:______。(用化学式表示)
【题目】实验室中分别用高锰酸钾、过氧化氢、氯酸钾制取比较纯净的氧气。请你按照要求回答问题:
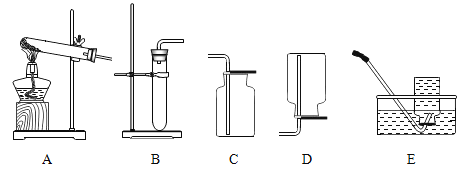
(1)结合图1所提供装置完成下列表格。
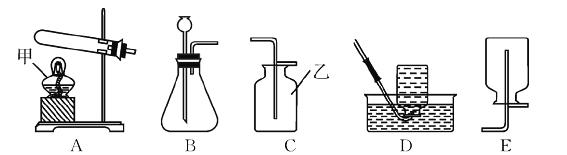
反应物填写内容 | 反应的文字表达式 | 气体制取装置组合(填序号) |
过氧化氢(二氧化锰) | 例:过氧化氢 | ____ |
高锰酸钾 | __________________ | ____ |
氯酸钾(二氧化锰) | _______________________ |
(2)请结合图1回答问题:
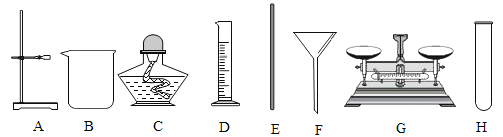
①写出甲、乙所指仪器名称:甲_____;乙_______;
②用过氧化氢制氧气的装置与其他两种方法的装置相比具有的优点是______、______ (写出两条);
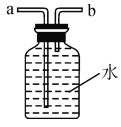
③若用图2装置收集一瓶氧气,气体应从______ (填“a”或“b”)端进入集气瓶。
(3)小柯为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,并使用传感器测定收集到的氧气浓度,数据见表。
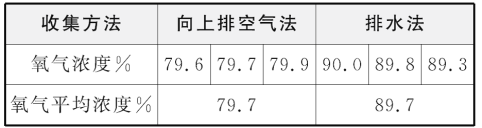
①小柯用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水法收集氧气时,以观察到______为氧气集满的标准。
②以上两种方法中,______法收集到的氧气更纯净。
③向上排空气法收集到的氧气浓度只有80%左右的原因有(_____)
A.氧气的密度略大于空气的密度
B.加热高锰酸钾固体产生氧气的浓度只有80%左右
C.当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
【题目】下表是![]() 和
和![]() 在不同温度时的溶解度,回答问题。
在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
I.两种物质中,溶解度受温度影响变化较大的是_____。
II.除去![]() 中少量的
中少量的![]() ,步骤是:加水溶解,蒸发浓缩,_____,过滤,洗涤,干燥。
,步骤是:加水溶解,蒸发浓缩,_____,过滤,洗涤,干燥。
III.50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:![]() 溶液_____(填“大于”、“等于”或“小于”)
溶液_____(填“大于”、“等于”或“小于”)![]() 溶液。
溶液。
IV.![]()

A中溶液_____(填“饱和”或“不饱和”)溶液,C中溶液的总质量是_____g。