题目内容
【题目】结合图示实验装置,回答下列问题。
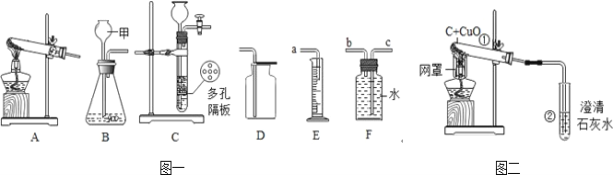
(1)实验室加热高锰酸钾制取氧气应选用的发生装置为___________(填字母),试管中棉花的作用是______________。
(2)若选B装置作为实验室制取氧气的发生装置,反应的化学方程式为:___________,某同学用D装置收集氧气,验满方法是___________。
(3)实验室可用B或C装置制二氧化碳,选用C相对于B装置的主要优点是___________。
(4)某同学用E、F装置收集一定量的氧气,装置接口连接的顺序为___________(填接口字母),量筒的作用是___________。
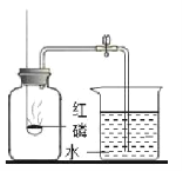
(5)图二中,酒精灯加网罩的目的___________。试管①中发生反应的化学方程式为:___________。
(6)图二实验停止加热时,应先将导管从试管②中撤出,并用弹簧夹夹紧橡皮管,待试管①冷却后再把试管里的粉末倒出,这样操作的原因是___________。
【答案】A 防止高锰酸钾粉末进入导气管 2H2O2 ![]() 2H2O + O2↑ 用带火星的木条放在集气瓶瓶口,若立即复燃,则已收满。 可以控制反应的发生与停止 ca 测量收集到的氧气体积 集中火焰,提升加热温度 C + 2CuO
2H2O + O2↑ 用带火星的木条放在集气瓶瓶口,若立即复燃,则已收满。 可以控制反应的发生与停止 ca 测量收集到的氧气体积 集中火焰,提升加热温度 C + 2CuO![]() 2Cu + CO2↑ 防止新生成的铜在高温下被空气中的氧气重新氧化成氧化铜
2Cu + CO2↑ 防止新生成的铜在高温下被空气中的氧气重新氧化成氧化铜
【解析】
图一(1)加热高锰酸钾制取氧气应选用固体受热发生装置,故填A;
加热高锰酸钾制取氧气时,试管口放一团棉花可以防止高锰酸钾粉末进入导管污染气体,故填防止高锰酸钾粉末进入导气管。
(2)B装置是过氧化氢分解制取氧气的发生装置故反应的化学方程式写为:2H2O2![]()
2H2O+O2↑;
用向上排空气法收集氧气时,验满的方法是用带火星的木条放在集气瓶瓶口,若木条复燃,则表明氧气已集满,故填用带火星的木条放在集气瓶瓶口,若木条复燃,则表明氧气已集满。
(3)C装置的优点是通过活塞的开闭可以控制反应的发生与停止,故填可以控制反应的发生与停止。
(4)用E、F装置收集一定量的氧气,由于氧气的密度小于水的密度,氧气应从短管进入瓶中,故填ca;
由图可知,排到量筒内的水的体积就是瓶中收集到氧气的体积,故填测量收集到的氧气体积。
图二(1)酒精灯加网罩可以集中火焰,提升加热温度,故填集中火焰,提升加热温度;
碳与氧化铜在高温的条件下反应生成二氧化碳和铜,故反应的化学方程式写为:C + 2CuO![]() 2Cu + CO2↑。
2Cu + CO2↑。
(2)上述操作可以防止新生成的铜在高温时被重新氧化为氧化铜,故填防止新生成的铜在高温时被空气中的氧气重新氧化成氧化铜。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案【题目】某实验小组的同学用氯化钙粉末、碳酸钠粉末、粒状大理石、稀盐酸、稀硫酸这几种药品,探究哪两种药品适合在实验室制取CO2。
请你参与下列的探究并回答问题。
(资料卡片)硫酸钙微溶于水,易在碳酸钙表面形成一层隔膜。
(提出问题)上述的酸和碳酸盐的反应是否适合在实验室制取CO2?
(方案设计)小红认为可选用稀硫酸、氯化钙反应制得CO2,小江认为不可能,小江的理由是_________。
大家经过讨论后,设计了如下三个实验进行对比分析。
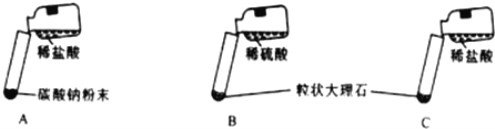
(实验与结论)(1)请你填写实验报告中①、②处的内容。
实验 | 实验现象 | 实验分析、结论 |
A | 剧烈反应,急速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
B | 产生气泡,速率迅速减慢,随后反应几乎停止 | 无法持续产生CO2,不能用于实验室制取CO2 |
C | 现象:_________ | 反应速率适中,气体便于收集 |
(2)根据探究结论,适合在实验室制取二氧化碳的是_______ (从A、B、C中选一种)。
(3)实验室不能用实验B制取二氧化碳的原因是______。
(拓展与迁移)(1)由上述探究可知,在确定实验室制取气体的反应原理时,要考虑诸多因素,例如反应速率要适中,便于收集等。请你再写出一种需要考虑的因素:_____ ,C+O2![]() CO2 是我们最熟悉的反应,生成物也只有CO2,为什么在实验室我们不利用碳的燃烧来制取CO2,其主要原因是_________。(答出1条)
CO2 是我们最熟悉的反应,生成物也只有CO2,为什么在实验室我们不利用碳的燃烧来制取CO2,其主要原因是_________。(答出1条)
(2)以下是某研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | H2O2溶 液浓度% | H2O2溶液体积/mL | 温度℃ | MnO2的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 |
| 2 | 49.21 |
④ | 30 | 5 | 55 |
| 2 | 10.76 |
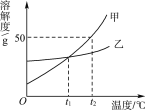
通过实验①和②对比可知,化学反应速率与_____有关;
从实验③和④对比可知,化学反应速率与温度的关系是:_________。
(3)某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.54 | 3.08 | 4.4 | m |
①哪几项反应中盐酸有剩余_____________;
②上表中m的数值是__________________;
③试计算这种石灰石矿中碳酸钙的质量分数_________。(要有完整的计算过程)
【题目】(1)黄铜是___________(填“Cu-Ag”或“Cu-Zn”)的合金。
(2)小桦和小杰对黄铜的成分产生兴趣,他俩决定对黄铜中的铜元素含量进行测定探究:
小桦称取10g黄铜样品,量取60g质量分数为14.6%的稀盐酸平均分成六等份,分别加入到盛有黄铜的烧杯中,当小杰观察到无气泡冒出时记录了以下表格数据:
次数 | 1 | 2 | 3 | 4 | 5 | 6 |
加稀盐酸质量(g) | 10 | 20 | 30 | 40 | 50 | 60 |
烧杯中固体质量(g) | 8.7 | 7.4 | 6.1 | 4.8 | 3.5 | 3.5 |
请回答下列问题:
①当反应到无气泡冒出时,所消耗的稀盐酸是____________g。
②生成氢气为多少_______ g?(写出计算过程)
③黄铜中铜元素的质量分数是_________________。
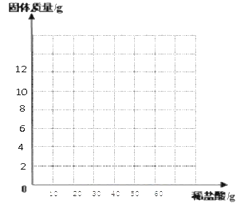
④画出黄铜的质量随加入稀盐酸的变化关系图:____________