题目内容
【题目】下列物质放入水中能形成溶液的是( )
A.牛奶 B.面粉 C.蔗糖 D.花生油
【答案】C
【解析】
试题分析:A.牛奶 B.面粉D.花生油都不溶于水,不能形成溶液;C.蔗糖能溶于水,形成均一、稳定的溶液

 阅读快车系列答案
阅读快车系列答案【题目】铜是一种常用的金属,纯净的铜颜色为紫红色,它能够和硝酸银溶液发生化学反应,生成硝酸铜和银单质。某同学设计下表所示实验,探究金属铜对过氧化氢溶液分解速率的影响。
操作 | 装置 | 现象 |
1、取一小块铜丝网,卷成筒形,固定在铜丝上。 |
|
|
2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中。 |
| 约1min后可观察到①和②中都有少量气泡产生 |
3、把铜丝插入①中。 |
| ①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生 |
(1)仪器②中实验的目的是__________________________;
(2)根据上述实验,可以得出的结论是______________________________;
(3)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是___________________。
A.称量实验前铜丝网的质量 B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰 D.将实验后的铜丝网插入AgNO3溶液中。
【题目】请结合下列实验常用装置,回答有关问题.
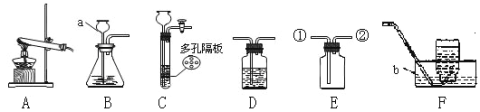
(一)(1)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为 ,若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放 试剂(填写试剂名称).如果用E装置收集该气体则气体从 端进入(填“①”或“②”)。
(2)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,难溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是 。
(二)实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示).
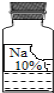
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
ⅡNa2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ室温(20℃)时,测定四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度g | 36 | 109 | 215 | 9.6 |
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验.
实验步骤 | 实验现象 | 结论及化学方程式 |
取少量溶液于试管中,滴加 | 产生大量气泡 | 反应的化学方程式: |
② 把产生的气体通入澄清的石灰水中. | 澄清的石灰水变浑浊 | 猜想②正确. 反应的化学方程式: |