题目内容
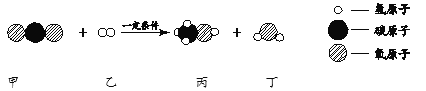
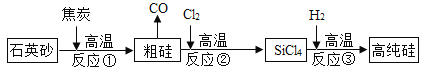
【题目】高纯硅可用于制备硅半导体材料.制备高纯硅的主要生产流程如图所示。
信息:石英砂的主要成分是SiO2,反应①化学方程式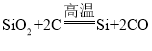
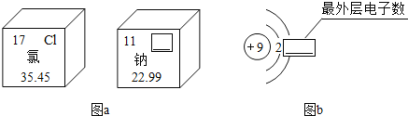
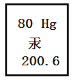
(1)石英砂属于_____(填“纯净物”或“混合物”);SiCl4中硅元素的化合价为____;写出合理处理中间产物CO的一种方法_________________.
(2)反应③反应除生成高纯硅外,同时还生成一种化合物.请写出此过程的化学方程式__________;
(3)反应③如果H2中混入O2,从安全角度考虑,可能引起的后果是_______________.
(4)写出氢气的用途________________________(填一种即可)
【答案】混合物 +4价 用酒精灯点燃 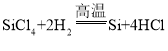 爆炸 冶炼金属;做燃料。
爆炸 冶炼金属;做燃料。
【解析】
(1)石英砂的主要成分是为二氧化硅,证明含有其他杂质,为混合物;在化合物中氯离子的化合价一般为-1价,设硅元素的化合价为x,由化合物中各元素的化合价代数和应为0,则有![]() ,解得x=+4,故SiCl4中硅元素的化合价为+4价;处理中间产物一氧化碳的方法可以为用酒精灯点燃;
,解得x=+4,故SiCl4中硅元素的化合价为+4价;处理中间产物一氧化碳的方法可以为用酒精灯点燃;
(2)反应③为与在高温条件下发生的反应,该反应除生成高纯硅外,同时还生成一种化合物,由质量守恒定律可知该化合物应为氯化氢,此过程的化学方程式为
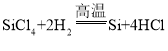 ;
;
(3)如果氢气中混入氧气,从安全角度考虑,可能引起的后果是爆炸;
(4)氢气具有还原性,可以用来冶炼金属;氢气是清洁能源,可以用来做燃料。

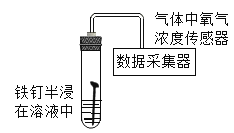
【题目】某研究小组为探究“铁钉在不同溶液中腐蚀的速率”,在相同条件下取同浓度的下列不同溶液用如图装置完成实验,并用手持数据采集器进行测定。回答下列问题:
所用溶液 | NH4Cl | (NH4)2SO4 | NH4NO3 |
0min时氧气浓度(%) | 20.8 | 20.8 | 20.8 |
500min时氧气浓度(%) | 15.8 | 17.0 | 17.4 |
实验前溶液PH | 5.31 | 5.53 | 5.50 |
实验后溶液PH | 7.37 | 7.99 | 8.22 |
铁钉表面锈蚀情况 | 大量铁锈 | 大量铁锈 | 大量铁锈 |
(1)用稀硫酸去除铁锈的化学反应方程式为_____
(2)在NH4Cl、(NH4)2SO4、和NH4NO3溶液中,铁钉锈蚀过程中上述溶液的酸性均变_____(填“强”或“弱”)
(3)上述实验方案是否合理?_____(填“合理”或“不合理”),你的理由是_____
(4)铁钉锈蚀的速率还可能与_____有关。请设计你的实验,验证你的猜想:
实验操作 | 实验现象及结论 |
_____ | _____ |
(注意:若答对第(5)小题奖励4分,化学试卷总分不超过60分)
(span>5)该小组在不同酸碱性溶液中又进行了探究,在相同条件下其测定的实验数据如下图:
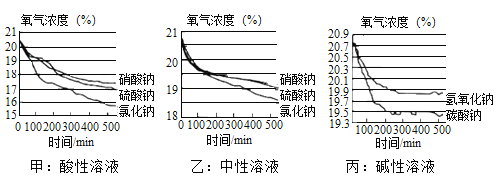
a、上述实验中,氧气浓度下降先陡后缓的原因为_____
b、根据甲、乙图像,请写出三点结论:
①结论:_____②结论:_____③结论:_____
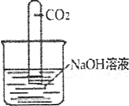
【题目】实验室用石灰水而不用氢氧化钠溶液鉴定二氧化碳。氢氧化钠能否与二氧化碳反应?
【查阅资料】Ⅰ.氢氧化钠溶液与二氧化碳反应生成易溶的碳酸钠,碳酸钠在二氧化碳过量的条件下继续与水和二氧化碳反应生成碳酸氢钠
Ⅱ.碳酸钠和碳酸氢钠性质对比如下表
操作 | NaHCO3溶液 | Na2CO3溶液 |
加入稀盐酸 | 产生气泡 | 产生气泡 |
加入稀CaCl2溶液 | 无明显变化 | __________________(填写现象)) |
加热溶液至沸腾,并将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
【进行实验】
实验操作 | 实验现象 | 结论及化学方程式 |
| ___________________ | 氢氧化钠与二氧化碳反应生成碳酸钠.反应方程式_______________ |
【实验反思】学习小组讨论,认为产生此实验现象的原因可能有两种:一种是NaOH与C02发生了反应;另一种是_______________
(2)为了进一步验证CO2与NaOH溶液已经发生反应,请你设计一个简单的实验检验生成的新物质。
实验步骤 | 实验现象 | 解释与结论 |
____________________________ | ____________________________ | NaOH与CO2发生了反应 |
【实验拓展】该小组同学将二氧化碳通入氢氧化钠溶液中,利用数字化技术测定溶液pH值变化,待完全反应后,观察到溶液中逸出大量气泡,pH出现两段S型变化曲线。

【实验分析】
(3)AB段变化的原因可能是________。BC段变化的原因可能是___________。利用实验验证变化后的产物,实验操作为_________________.实验现象是____________________。
【题目】以下是我们日常生活中常用的清洗剂,其名称及有效成分如下表:
![]()
![]()

| 洁厕灵 |
| 污渍爆炸盐 |
有效成分 | 盐酸 | 过氧化氢 | 过碳酸钠 |
(1)清除以下物质,可以使用洁厕灵的是________(填字母序号)。
A.铁锈 B.水垢(主要成分为碳酸钙和氢氧化镁) C.油渍
(2)“活氧彩漂”可用于漂洗衣物、杀菌消毒等,原因是其有效成分过氧化氢分子中含有“过氧基”(—O—O—)。据此推测,下列物质中,可用作杀菌消毒剂的是________(填序号)。
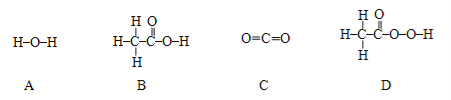
(3)“污渍爆炸盐”溶于水,生成Na2CO3和H2O2。再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,写出产生此气体的化学方程式________。