题目内容
【题目】一密闭容器中有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质 | X | Y | M | N |
反应前质量/g | 3 | 5 | 15 | 42 |
反应后质量/g | 3 | 待测 | 28 | 16 |
下列说法正确的是
A.待测值为8
B.X一定是该反应的催化剂
C.该反应类型为化合反应
D.参加反应的M和N的质量比为1:2
【答案】D
【解析】
A、由于反应是在密闭容器中进行的,根据质量守恒定律,反应前后物质的总质量应相等。设待测值为x,则![]() ,解得
,解得![]() ,待测值为18,故选项错误;
,待测值为18,故选项错误;
B、根据表中数据可知,X反应前后质量不变,则X可能是该反应的催化剂也可能是未参与反应的杂质,故选项错误;
C、Y、M反应后质量增加,为生成物,N反应后质量减少,为反应物,可知该反应为分解反应,故选项错误;
D、参加反应的M的质量为![]() ,N的质量为
,N的质量为![]() ,故参加反应的M和N的质量比为1:2,故选项正确。故选D。
,故参加反应的M和N的质量比为1:2,故选项正确。故选D。

【题目】下列我国科技成果所涉及物质的应用中,体现物质物理性质的是
|
|
|
|
A 利用石墨烯优异的导电性,制成新型电阻触摸屏的电极 | B可燃冰是天然气水合物,作为新能源使用 | C 甲醇(CH3OH)低温制得氢气,用于新能源汽车 | D 优化煤的综合利用,发展煤制乙醇(C2H5OH)技术 |
A.AB.BC.CD.D
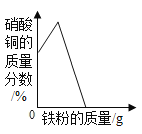
【题目】某兴趣小组同学在做金属与盐溶液反应的实验时,发现钠放人硫酸铜溶液后,并没有红色固体析出,而是溶液中有无色气泡和蓝色沉淀生成。同学们对产生这--异常现象的原因进行探究。
同学们将充分反应后的混合物过滤,得到无色滤液A。
[查阅资料]钠与水反应生成氢氧化钠。写出氢氧化钠与硫酸铜反应的化学方程式_________________________。
[进行实验]同学们对产生的气体和无色滤液A的成分进行如下探究。
实验探究 | 甲组 | 乙组 |
[提出问题] | 产生的气体是什么? | 无色滤液A的溶质成分是什么? |
[作出猜想] | 猜想一:H2 猜想二:O2 猜想三:CO | 猜想①:Na2SO4 猜想②:Na2SO4、NaOH 猜想③:Na2SO4、CuSO4 |
[实验验证] | 小丽认为不可能生成CO,理由 是_____________________________。小英收集一试管产生的气体,管口向下移近酒精灯火焰,听到尖锐的爆鸣声 | 取少量无色滤液A于试管中,向其中滴加几滴无色酚酞溶液,观察到________________________。 |
[实验结论] | 猜想______________________成立 | 猜想②成立 |
[反思交流]小明认为无需实验证明,滤液A中一定没有CuSO4,原因是________________________。
[拓展应用]用硫酸铜和石灰水配制农药波尔多液时,不能用________________________(填字母)容器盛放。
A 铜制容器
B 瓷制容器
C 铁制容器
D 玻璃容器
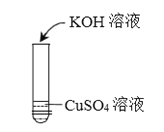
【题目】某兴趣小组在实验室中探究氢氧化钾的性质,请你参与他们的探究。
(实验过程与分析)
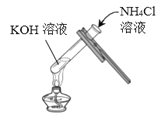
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | _______ | ______ | 无明显现象 |
实验结论 | 氢氧化钾能与硫酸铜发 生反应 | 氢氧化钾能与氯化铵发 生反应 | 氢氧化钾不能与硫酸 发生反应 |
(实验反思与拓展)
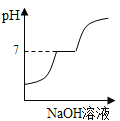
①某同学认为实验三的结论不正确。他改进了该实验方案,借助于酸碱指示剂,通过明显的现象证明氢氧化钾能与硫酸发生反应。简述他的实验方案:_____(写出操作方法和现象)。
②对于无明显现象的化学反应,可通过检验有新物质生成或检验_____的方法来证明物质间发生了化学反应。