题目内容
【题目】工业上常采用“天然苛化法”制取氢氧化钠,部分流程如下:
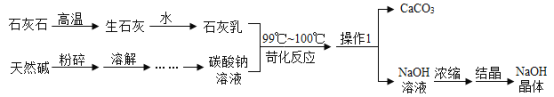
(1)操作1的名称是__。
(2)写出石灰石在高温条件下发生反应的主要化学方程式:__,苛化反应属于__(填基本反应类型)。
(3)工艺中采用石灰乳而不用氢氧化钙溶液与碳酸钠反应的原因是__。
(4)生产工艺中可以循环再利用的物质是__。
(5)由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的是__。
【答案】过滤 CaCO3![]() CaO+CO2↑ 复分解反应 氢氧化钙微溶于水,溶液中氢氧化钙的含量低 碳酸钙 加快溶解速率
CaO+CO2↑ 复分解反应 氢氧化钙微溶于水,溶液中氢氧化钙的含量低 碳酸钙 加快溶解速率
【解析】
(1)操作1将固体与液体分离,其名称是过滤。
(2)石灰石在高温条件下发生反应生成氧化钙和二氧化碳,反应的主要化学方程式为:CaCO3![]() CaO+CO2↑;根据流程图可知,苛化反应是氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙,该反应是由两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应。
CaO+CO2↑;根据流程图可知,苛化反应是氢氧化钙与碳酸钠反应生成氢氧化钠和碳酸钙,该反应是由两种化合物相互交换成分,生成另外两种化合物的反应,属于复分解反应。
(3)工艺中采用石灰乳,而不用氢氧化钙溶液与碳酸钠反应的原因是氢氧化钙微溶于水,溶液中氢氧化钙的含量低。
(4)根据流程图可知,碳酸钙既是反应物又是生成物,生产工艺中可以循环再利用的物质是碳酸钙。
(5)由天然碱得到碳酸钠溶液时,将天然碱粉碎的目的是加快溶解速率。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】过碳酸钠俗称固体双氧水,其化学式为Na2CO4,广泛应用于洗涤、印染、纺织、造纸等领域。某化学兴趣小组同学取一定量的过碳酸钠样品,加入一定量的稀硫酸,发现产生大量气泡,同时得到无色溶液。同学们对得到的无色溶液中的溶质成分进行以下探究。
(温馨提示:实验中若涉及硫酸钙等微溶物,均视为可溶物)
[提出问题]溶液中溶质的成分是什么?
[查阅资料]过碳酸钠与水反应有两个过程:①![]() ;②过氧化氢在碳酸钠水解产生的氢氧根离子的催化作用下分解为水和氧气。
;②过氧化氢在碳酸钠水解产生的氢氧根离子的催化作用下分解为水和氧气。
[猜想与假设]
猜想一:Na2SO4;
猜想二:________________________________。
猜想三:Na2SO4、H2SO4;
猜想四:Na2SO4、H2SO4、Na2CO3。
其中不合理的猜想是_______________________,理由是_______________________。
[实验探究]
实验方案 | 实验操作 | 实验现象 | 实验结论 |
方案一 | 取少量溶液于试管中,滴加氯化钡溶液 | 有白色沉淀产生 | 猜想一成立 |
方案二 | 取少量溶液于试管中,滴加_______________溶液 | 有白色沉淀产生 | 猜想二成立 |
方案三 | 另取少量溶液于试管中,加入铁粉 | _______________________ | 猜想三不成立 |
[反思与评价]某同学提出,实验方案一不严谨,不能证明猜想一成立,原因是_______________________。
[拓展延伸]过碳酸钠在运输、保存中不能接触的物质有_______________________(填字母)。
A.稀盐酸
B.水
C.氯化钙溶液
D.氯化钠固体
【题目】“微观、宏观、符号”是化学学科的三大特征
第一周期 | 1H | 2He | ||||||
第二周期 | 3Li | 4Be | 5B | ① | 7N | 8O | 9F | 10Ne |
第三周期 | ② | 12Mg | 13Al | 14Si | 15P | ③ | 17Cl | 18Ar |
分析以上元素周期表,回答下列问题
(1)“6000L氧气在加压下可装入容积为40L的钢瓶中”是因为_____。
(2)画出①所示的原子结构示意图_____。
(3)地壳中含量最多的金属元素位于周期表的第_____周期。
(4)②所示元素与③所示元素形成化合物的化学式是_____。
(5)请写出碳不充分燃烧的化学方程式_____。
【题目】一密闭容器中有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:
物质 | X | Y | M | N |
反应前质量/g | 3 | 5 | 15 | 42 |
反应后质量/g | 3 | 待测 | 28 | 16 |
下列说法正确的是
A.待测值为8
B.X一定是该反应的催化剂
C.该反应类型为化合反应
D.参加反应的M和N的质量比为1:2