题目内容
【题目】(12分)以下是日常生活中常用各种清洗剂。

(1)使用洗涤灵清洗餐具上的油污,这是因为它具有 功能。
(2)清除以下物质,可使用炉具清洁剂的是 (填字母序号)。
A.铁锈 B.油污 C.水垢
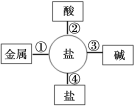
(3)“污渍爆炸盐”溶于水后会生成Na2CO3和H2O2。将爆炸盐溶于水后,再加入足量的洁厕灵,产生能使澄清石灰水变浑浊的气体,此反应
体现了下图中 (选填①②③④)性质关系。
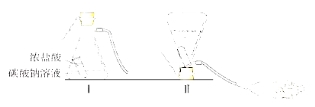
(4)将洁厕灵滴入炉具清洁剂中,如下图甲所示。
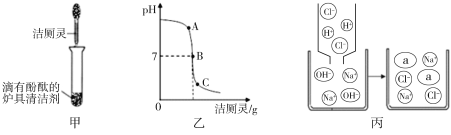
①若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外) ,此时溶液可用图乙中 (选填A、B、C)点处表示。
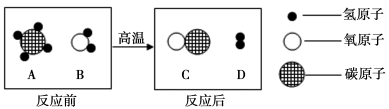
②若反应后溶液pH为7,图丙中a微粒的化学式为 。
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有 。
A.无色酚酞溶液 B.硝酸钾溶液 C.硝酸银溶液 D.锌粒
(5)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放。
某造纸厂废水中含NaOH的质量分数为l.6%,现有废硫酸9.8t(H2SO4的质量分数为20%),可处理的废水质量是多少?(写出计算过程)
【答案】(1)乳化
(2)B
(3)②
(4)①NaCl、NaOH A ②H2O ③AD
【解析】
试题分析:(1)洗涤剂具有乳化作用,能将大的液滴分散成小液滴除去;
(2)炉具清洁剂的主要成分是氢氧化钠,氢氧化钠只能与油污发生反应,故选B;
(3)洁厕灵的主要成分是盐酸,盐酸能与碳酸钠反应生成二氧化碳,二氧化碳能使澄清石灰水变浑浊。碳酸钠属于盐,盐酸属于酸,故是盐与酸的反应,选②;
(4)炉具清洁剂的主要成分是氢氧化钠,洁厕灵的主要成分是盐酸,盐酸能与氢氧化钠发生中和反应生成氯化钠和水;碱能使酚酞试液变成红色,酸性和中性溶液均不能使酚酞变色,若反应后溶液呈红色,说明溶液呈碱性,即氢氧化钠溶液过量,故反应后溶液中的溶质是NaCl、NaOH,此时溶液可用图乙中的A点表示;若反应后溶液pH为7,说明氢氧化钠和盐酸恰好完全反应,那么溶液中只有氯化钠和水,故a是水;氢氧化钠与盐酸反应生成氯化钠和水的过程中没有任何现象,要证明它们发生了反应,可通过证明氢氧化钠或盐酸的存在即可,故选AD;
(5)利用化学方程式,根据反应的质量比即可计算出氢氧化钠的质量。
解:9.8t废硫酸中含硫酸的质量为:9.8t×20%=1.96t
设9.8t废硫酸可反应的NaOH的质量为x。
H2SO4 +2NaOH==Na2SO4+2H2O
98 80
1.96t x
x=1.6t
1.6t÷1.6%=100t
答:可处理的废水质量是100t。

 名校课堂系列答案
名校课堂系列答案【题目】(17分)实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面有白色粉末。某兴趣小组的同学对该样品的成分及含量进行了探究。
【提出问题1】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3。
(1)则NaOH变质反应的化学方程式为 。
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应。
②二氧化碳在饱和的碳酸氢钠溶液中几乎不溶解,在27℃、101kPa时的密度为1.8 g·L-1。
【实验探究1】
(2)为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告。
实验操作 | 实验现象 | 实验结论 |
(a)取少量样品溶于水,加入 ; | 有白色沉淀产生 | 该反应的化学方程式为 |
(b)静置,向 。 | 证明猜想Ⅱ成立 |
【提出问题2】如何测量该部分变质样品中碳酸钠的质量分数?
【实验探究2】
小红同学设计了如下图所示的装置(铁架台略去),在27℃、101kPa下按下列步骤进行实验:
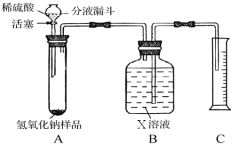
①按图连接好装置;
②用托盘天平准确称取该样品2g,放入A中试管内,向B中集气瓶中倒入X溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到X溶液220mL。
(3)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是 。
(4)B中集气瓶盛装的X溶液应为 溶液。
(5)试管中原有的空气对实验结果 (选填“有”或“没有”)明显影响。
(6)变质氢氧化钠样品中碳酸钠的质量分数为 (精确至1%)。
【提出问题3】怎样提纯该样品得到较纯净的氢氧化钠固体?
【实验探究3】
为了得到较纯净的氢氧化钠固体,小亮明设计了如下图所示的实验流程。
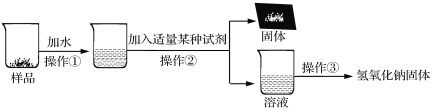
(7)操作②的名称是 ,为了使样品充分溶解,操作①中还要用到的玻璃仪器是 。
(8)该实验中发生反应的化学方程式为 。
(9)最终所得氢氧化钠固体的质量 变质样品中氢氧化钠的质量(选填“大于”、“等于”或“小于”)。
【反思与交流】
(10)敞口放置的氢氧化钠溶液容易变质,所以试剂瓶要 塞密封保存。
(11)通过本题,你学会了定性检验氢氧化钠的变质、定量测定变质后某成分的含量,以及除杂提纯物质。为了得到可靠的实验结果,探究过程中你需要思考问题有 (填数字序号);
①选择试剂种类
②确定试剂用量
③试剂产地
④实验装置与步骤的设计
⑤实验安全环保
⑥测量中减少误差
(12)【实验探究1】中的检验和【实验探究3】中的除杂都将碳酸钠进行了转化,但二者目的不同,它们分别是 。