题目内容
【题目】图1是利用数字化仪器测定CO2含量的探究实验。
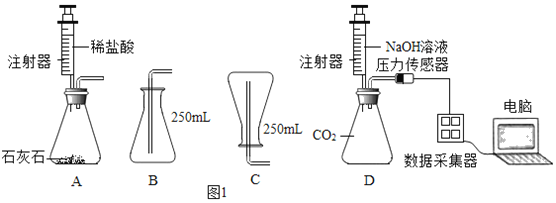
(1)按照图A所示连接实验装置,检查该装置气密性的方法是_____。
(2)用装置A制取CO2气体,并分别用排液体法和排空气法收集两锥形瓶气体备用,制取CO2的化学反应方程式为_____。
(3)采取D图装置,将注射器中等量、等浓度的氢氧化钠溶液分别注入用排液体法和排空气法收集的CO2气体的锥形瓶内(NaOH溶液均过量),得到如图2所示的压强随时间变化的曲线图。请用化学方程式说明锥形瓶内压强变化的原因。_____
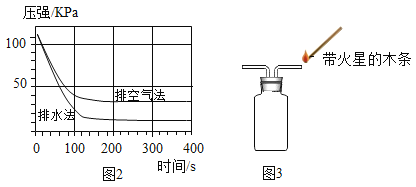
(4)该实验说明_____收集到CO2的含量较高(填“排液体法”或“排空气法”),请结合图说明你的理由:_____。
(5)利用图A、B装置还可制取一种常见的气体,写出反应的化学方程式_____。若用图3装置采用排空气法收集氧气,请将B装置中导管补画完整_____。
(6)加热30g氯酸钾和二氧化锰的固体混合物制取氧气,待反应完全后,可以得到20.4g固体物质。请计算原固体混合物中二氧化锰的质量_____。
【答案】用止水夹夹紧胶皮管,轻推或轻拉注射器活塞,松开活塞后,如果活塞回到原来的位置,则气密性良好 CaCO3+2HCl=CaCl2+H2O+CO2↑ 2NaOH+CO2=Na2CO3+H2O 排液体法 注入氢氧化钠溶液后,排液法收集到的气体,锥形瓶内压强变化较大 2H2O2![]() 2H2O+O2↑
2H2O+O2↑ 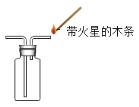 5.5g
5.5g
【解析】
(1)按照图A所示连接实验装置,首先要形成密闭空间,所以用止水夹夹住胶皮管,然后通过推拉注射器的活塞,看密闭空间的压强,具体检查该装置气密性的方法是:用止水夹夹紧胶皮管,轻推或轻拉注射器活塞,松开活塞后,如果活塞回到原来的位置,则气密性良好;故填:用止水夹夹紧胶皮管,轻推或轻拉注射器活塞,松开活塞后,如果活塞回到原来的位置,则气密性良好
(2)实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;故填:CaCO3+2HCl=CaCl2+H2O+CO2↑
(3)二氧化碳和氢氧化钠反应生成碳酸钠和水,使锥形瓶内压强降低,化学方程式为:2NaOH+CO2=Na2CO3+H2O;故填:2NaOH+CO2=Na2CO3+H2O
(4)由图排液法收集的二氧化碳引起的压强变化明显,说明该实验排液法收集到CO2的含量较高,理由:注入氢氧化钠溶液后,排液法收集到的气体,锥形瓶内压强变化较大;故填:排液体法;注入氢氧化钠溶液后,排液法收集到的气体,锥形瓶内压强变化较大
(5)根据装置的特点可知,制取气体不需加热,气体的密度比空气大,可用过氧化氢分解制取氧气,故化学方程式为:2H2O2![]() 2H2O+O2↑;将B装置中导管补画完整如图:
2H2O+O2↑;将B装置中导管补画完整如图: ;故填:2H2O2
;故填:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(6)生成氧气的质量为:30g﹣20.4g=9.6g。设生成9.6g氧气需要氯化钾的质量为x
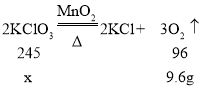
![]()
x=24.5g
原固体混合物中二氧化锰的质量为:30g﹣24.5g=5.5g
答:原固体混合物中二氧化锰的质量为5.5g。故填:5.5g

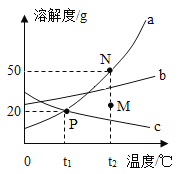
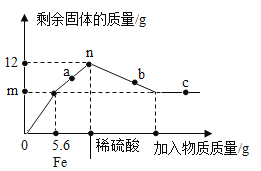
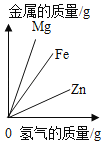
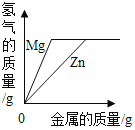
【题目】下列图象能正确反映对应变化关系的是( )
|
|
|
|
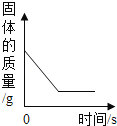
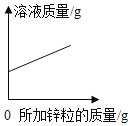
Mg、Zn、Fe与稀盐酸反应 | 等质量等质量分数的盐酸与足量的镁粉、锌粉 | 将铜片加入一定量的硝酸银溶液中 | 向一定质量的氯化锌和盐酸溶液中加入锌粒 |
A. A B. B C. C D. D