��Ŀ����
����Ŀ��������;ʮ�ֹ㷺���ι����ս�����֪ʶ���б�Ҫ��
��1�����й��ڽ�����˵���в���ȷ����___________
A�����������������ɫ�� B���ǵؿ��к�����ߵĽ���
C��Ļ�ԱȽ��� Dˮ���ڳ�������Һ��
��2�������������Ϊͭ������ͭ��ԭ�������û�ѧ����ʽ��ʾ��ԭ��_____________��
��3�����ڽ������˳����λ����ǰ�棬��С�ַ�������ϡ���Ὺʼ��Ӧʱ�������漸��û�����ݲ���������������������ԭ��д����صĻ�ѧ����ʽ______________��
��4����Mg(NO3)2��Cu(NO3)2�Ļ����Һ�м�������Ϊa g��Zn�ۺ�Fe�ۣ���ַ�Ӧ����ˣ�������ϴ��������������������Ϊa g��ͬѧ�Ƕ������ijɷ��������룺����٣�Cu������ڣ�Fe��Cu������ۣ�Zn��Fe��Cu
���������ۣ�ͬѧ��һ����Ϊ����_____________�������������ǣ�____________________��
��5��ͭ�Ľ��������Ȼλ����֮����������ʾͭ���Ժ�ϡ���ᷴӦ���仯ѧ����ʽΪ3Cu��8HNO3��3Cu(NO3)2��4H2O��2M����M�Ļ�ѧʽΪ____________��
��6���ֽ�1.92gͭ�ӵ�50gϡ�����У�ǡ����ȫ��Ӧ����ϡ���������ʵ���������_____________��
���𰸡�B Fe + CuSO4=Cu + FeSO4 ���ı����γ���һ�����ܵ�����Ĥ��4Al+3O2=2Al2O3��Al2O3+6HCl�T2AlCl3+3H2O �� ���μӷ�Ӧʱп�Ѿ���ȫ��Ӧ NO 10.08%
��������
��1��A�������������������ɫ�ģ���ȷ��
B�����ǵؿ��к�����ߵĽ����������ǡ�����
C����Ļ�ԱȽ�������ȷ��
D��ˮ���ڳ�������Һ�壬��ȷ��
��ѡ��B��
��2�������������Ϊͭ������ͭ��ԭ����������ͭ������Ӧ��������������ͭ����Ӧ�Ļ�ѧ����ʽΪ��CuSO4+Fe=FeSO4+Cu��
��3�����ڽ������˳����λ����ǰ�棬��������Ϊ���ã�������������Ӧ����������������������ϡ���ᷴӦ���������ɣ���������Ӧ��ȫ������ϡ���ᷴӦ�������������
��4����Ӧ�����Ļ��˳��ΪMg��Zn��Fe��Cu����Mg��NO3��2��Cu��NO3��2�Ļ����Һ�м�������Ϊag��Zn�ۺ�Fe�ۣ�����п�������ã�����п��ȫ��Ӧ�����ܺ�����ͭ��Ӧ����п������ͭ��Ӧ������������٣�����������ͭ��Ӧ���¹����������ӣ�����ַ�Ӧ����ˣ�������ϴ��������������������Ϊag��˵����Ҳ�μ��˷�Ӧ������Ӧ�ô�ʱп�Ѿ���ȫ��Ӧ�����Բ��� �۲������������ǣ����μӷ�Ӧʱп�Ѿ���ȫ��Ӧ
��5��3Cu+8HNO3=3Cu��NO3��2+4H2O+2M����Ӧǰ��Cu 3����H 8����N 8����O 24������Ӧ������Cu 3����H 8����N 6����O 22����ȱ��N 2��O 2������M �Ļ�ѧʽΪNO��
��ϡ���������ʵ���������Ϊx
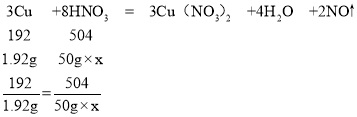
x=10.08%
�ʴ�Ϊ��
��1��B��
��2��CuSO4+Fe=FeSO4+Cu��
��3�����ı����γ���һ�����ܵ�����Ĥ��4Al+3O2=2Al2O3��Al2O3+6HCl�T2AlCl3+3H2O��
��4���ۣ����μӷ�Ӧʱп�Ѿ���ȫ��Ӧ
��5��NO��10.08%��

����Ŀ��ij��ѧ��ȤС����һ��ʵ���н�����ͼ��ʾ��ʵ�飺

��ʱ�۲쵽U�ι�������������������Dz�ͬ�ģ�ʵ���С��ͬѧ�����U�ιܡ����ֹ������а�ɫ�������������������ͬѧ�Ƕ���Һ�ɷֲ���Ũ�����Ȥ�����ǽ����˽�һ����̽���
��1����������⣩��Һ�п��ܺ�����Щ���ʣ�
����������裩����һ������ΪNaCl
�����������ΪNaCl��BaCl2
������������ΪNaCl��BaCl2��HCl
����Ϊ���ϲ���_____��������������_____�����û�ѧ����ʽ��ʾ������д����IJ���_____��
��2����ʵ��̽����С��Ϊ����֤��Һ�ɷ֣�ȡ��Һ���Թ��У������еμ���������������Һ���۲쵽�����������ɴ˵ó����ۣ�����һ������С����ΪС��Ľ����Ƿ�����_____������ܡ����ϡ�����
Ϊ����֤��IJ��룬����д�±���
ʵ����� | ʵ������ | ʵ����� |
ȡ��Һ�������Թ��У������еμ�����_____��Һ | ��Һ����ɫ��Ϊ��ɫ | ��IJ������ |
��3�����������ܽᣩͨ������ʵ�飬�����ܹ��ܽ������ȷ����ѧ��Ӧ��������Һ���ʳɷ�ʱ�����˿����������⣬����Ҫ����_____��
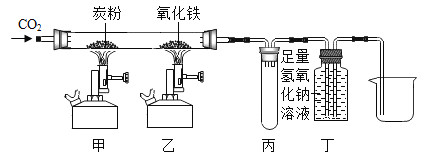
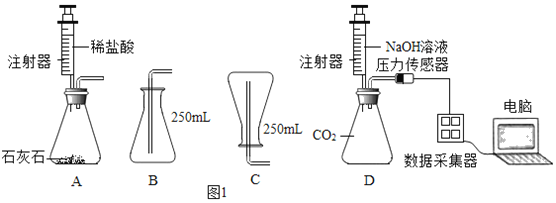
����Ŀ��˫��ˮ��H2O2������������������ҵ�г�ȥɫ�ߣ�Ҳ�����ڳ������Զ�������Ϊ���������ֽⷴӦ��ȡ������ijͬѧ�������ͼװ����ȡ�±��е����ִ�������������壮
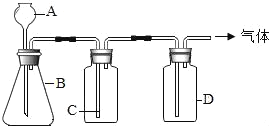
��A��B��C��D��ʾ��Ӧ�����м�����Լ���
���� | A | B | C | D |
O2 | ˫��ˮ��Һ | �������� | ˮ | �������ƹ��� |
H2 | ϡ���� | ͭ | ����������Һ | Ũ���� |
CO2 | ϡ���� | ����ʯ | ����������Һ | Ũ���� |
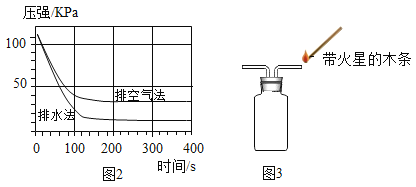
�����������п��Եõ��Ĵ����������������_____���ѧʽ����װ��D������ҩƷ��������_____���森
��ָ�����������������õ������壬��˵�����ɣ�����ѡһ�֣�����_____��������_____��