题目内容
【题目】下图是碳酸钠和氯化钠的溶解度曲线,下列叙述错误的是:
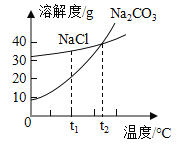
A.t1℃时,NaCl的溶解度大于Na2CO3的溶解度
B.t2℃时,NaCl和Na2CO3溶液中溶质质量分数一定相等
C.t1℃时,将NaCl的饱和溶液加热蒸发,一定有晶体析出
D.Na2CO3固体中含有少量的NaCl,可用降温结晶的方法提纯Na2CO3
【答案】B
【解析】
A、根据碳酸钠和氯化钠的溶解度曲线,t1℃时,NaCl的溶解度大于Na2CO3的溶解度,不符合题意;
B、t2℃时,没有指明溶液的状态,NaCl和Na2CO3溶液中所含溶质质量分数不一定相等,符合题意;
C、t1℃时,将NaCl的饱和溶液加热蒸发,一定有晶体析出,不符合题意,不符合题意;
D、碳酸钠和氯化钠两种固体物质的溶解度,都是随温度升高而增大,而碳酸钠的溶解度随温度的升高变化比氯化钠大,所以Na2CO3固体中含有少量的NaCl,可用降温结晶的方法提纯Na2CO3,不符合题意。故选B。

练习册系列答案
相关题目