题目内容
【题目】溶液是初中化学学习的主要内容之一。
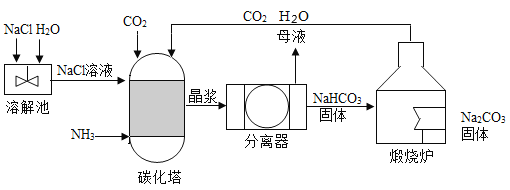
(1)配制一定质量分数的氯化钠溶液时,写出一条会导致溶液的质量分数偏小的操作___________。
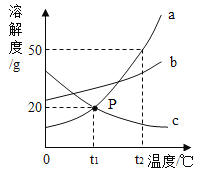
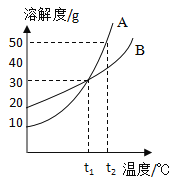
(2)如图是A、B的溶解度曲线。A和B的溶解度相等时的温度为______________;t2°C时,将30gA的饱和溶液稀释为质量分数为10%的溶液,需加水的质量为_____ g。
【答案】转移氯化钠固体至烧杯的过程中有固体洒出或用量筒量水时仰视刻度 t1℃ 70
【解析】
(1)配制一定质量分数的氯化钠溶液时,在转移氯化钠固体至烧杯的过程中有氯化钠固体洒出,会造成最终溶液中溶质的质量偏小,会导致溶液的质量分数偏小;在量取水的操作中仰视刻度读数,会造成量取水的体积偏大,会导致溶液的质量分数偏小。
(2)根据是A、B的溶解度曲线图可知,温度为t1°C时,A和B的溶解度曲线出现交点,说明该温度时A和B的溶解度相等;
t2°C时,A的溶解度为50g,说明该温度下100g水中溶解50gA达到饱和,将30gA的饱和溶液稀释为质量分数为10%的溶液,设需加水的质量为x,根据稀释前后溶质的质量保持不变,则有![]() ,解得x=70g,故需要加水的质量为70g。
,解得x=70g,故需要加水的质量为70g。

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目