��Ŀ����
����Ŀ��ij��ѧ��ȤС����������ʵ����̽�� CO2�������ȡ�����ʡ�
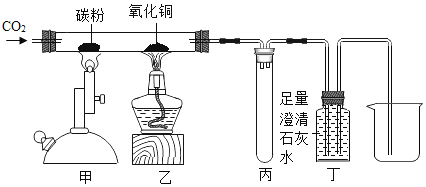
��ʵ������ȡCO2���塣
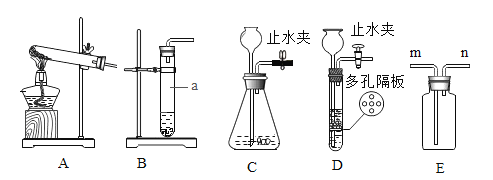
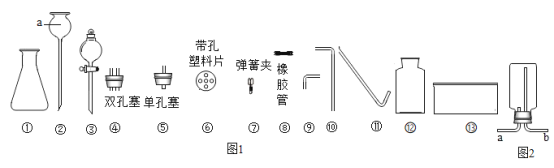
������a��������_____��
������ʵ������ȡCO2�ķ���װ����_____�����ţ����ռ�CO2Ӧ��E ��_____�����ӣ�ѡ����m������n������
������Cװ����ȡ����ʱ����Ӧδֹͣǰ�ر�ֹˮ�У��ɹ۲쵽��������_____��
��Dװ�������巢��װ�õ����÷�Χ��_____����Bװ����ȣ�����Dװ����ȡ������ŵ���_____��
���ÿ�״��ʯ��ʯ�����ϡ���ᷴӦ��ȡCO2�����μӷ�Ӧ��ʯ��ʯ�Ĵ���80%������Ϊ125g����Ӧ���� CO2 �����ʵ���Ϊ_____mol�����ݻ�ѧ����ʽ��ʽ���㣩��
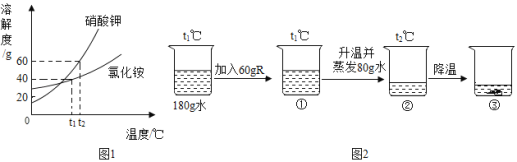
��̽��CO2�����ʡ�ʵ�鲽�����£�
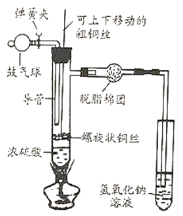
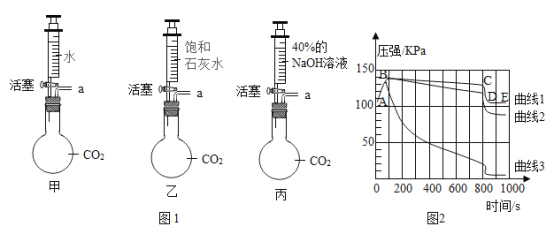
���� 1����ͼ1��ʾװ�õ����������ã�ͼ�� a ����������ѹ�������������ס��ҡ���������ƿ���ݻ���Ϊ250mL���ֱ��ռ���CO2������ע�����ڸ�װ��85mLҺ�塣
���� 2����λͬѧͬʱѸ�ٽ�ע������Һ��ȫ��ע�������ƿ�У��رջ�����һ��ʱ���ͬʱ����ƿ��
���� 3�����������ֻ�ʵ�����ⶨ��ƿ�ڵ���ѹ�仯���õ���ͼ2��ʾ����ƿ��ѹǿ��ʱ��Ĺ�ϵ����ͼ������ 1��2��3�ֱ��ʾ�ס��ҡ���������ƿ�ڵ���ѹ�仯��
��ʵ������У��۲쵽��ƿ�����а�ɫ�������ɣ��÷�Ӧ�Ļ�ѧ����ʽ_____��
��ͼ 2��AB����ѹ���������ԭ����_____�� ����1�е���CD����ѹ���ٱ�С�IJ�����_____��
�۶Ա����� 1 ������3���ܵó��Ľ�����_____������ţ���
a CO2������ˮ
b CO2����ˮ������Ӧ
c CO2����NaOH��Һ������Ӧ
�ܶԱ�����2������3�������ѹ�仯��������Ҫԭ����_____��
���𰸡��Թ� BCD n ����©��������һ��Һ�� ��״������Һ�峣���·�Ӧ�������� ������ͣ�����Ʒ�Ӧ�Ľ�����ֹͣ) 1 CO2+Ca��OH��2��CaCO3��+H2O ע�����е�Һ��Ѹ�ټ�����ƿ�� �� ac ��������������ˮ������ʯ��ˮ������������Һ�������������ն�����̼���
��������
��1��������a���������Թܣ�
��ʵ������ȡCO2�����ڳ����£��ô���ʯ��ʯ��ʯ��ϡ������ȡ�ģ�̼��ƺ����ụ�ཻ���ɷ������Ȼ��ƺ�ˮ�Ͷ�����̼������Ҫ���ȣ�����װ��ѡ��BCD��������̼������ˮ���ܶȱȿ������ܶȴ�ֻ���������ſ������ռ���Ӧ��E��n������
������Bװ����ȡCO2ʱ����Ӧδֹͣǰ�ر�ֹˮ�У�����װ���ڼ�����Ӧ����������̼���װ���ڵ�ѹǿ���۲쵽����©���ڵ�Һ��������
��Dװ���ǿ�״������Һ���ڳ����·�Ӧ��ȡ����ķ���װ�ã���װ��D�У�����ҩƷ���ڶ�����ϣ�Һ��ҩƷ�ӳ���©���м��롣��Ӧ��رտ���ʱ���Թ��е��������࣬ѹǿ����Һ��ѹ�볤��©���������Һ����룬��Ӧֹͣ������ʱ�����嵼�����Թ��е�������٣�ѹǿ��С��Һ������ϣ���Ӧ���С���Aװ����ȣ�����Dװ����ȡCO2���ŵ��ǿ���ʹ��Ӧ��ʱ��������ʱֹͣ��
���裺���ɶ�����̼�����ʵ���Ϊx
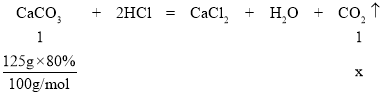
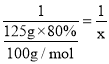
x��1mol
��2���ٶ�����̼���������Ʒ�Ӧ����̼��ư�ɫ������ˮ����ѧ����ʽΪ��CO2+Ca��OH��2��CaCO3��+H2O��
��ͼ 2��AB����ѹ���������ԭ����ע�����е�Һ��Ѹ�ټ�����ƿ�У�����ѹ������ѹ��������1�仯������С������װ�üף�BC����ѹ��С��ԭ���Ƕ�����̼����ˮ������ƿʹ������̼��Ӧ�����ʼӿ죬����������С������ѹǿ��С�����Ե���CD����ѹ���ٱ�С�IJ�������
��a������1����������ѹ���ͣ�˵��CO2������ˮ��a��ȷ��
b������1������3������˵��CO2����ˮ������Ӧ��b����
c������1������3�Աȣ�����3��ѹ�������ԣ�˵��CO2����NaOH��Һ������Ӧ��c��ȷ��
��ѡac
�ܶԱ�����2������3�������ѹ�仯��������Ҫԭ���� ��������������ˮ������ʯ��ˮ������������Һ�������������ն�����̼���