题目内容
如图1是小华同学用氢氧化钠固体和水配制50g溶质质量分数25%的NaOH溶液的操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把药品直接放在纸上称量.
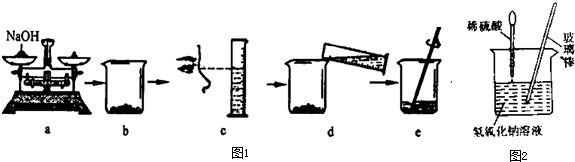
(1)a操作中的错误是______.
(2)下列操作中导致溶质质量分数偏低的是______(填字母).
A.a操作中砝码和氢氧化钠放错盘 B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为37.5ml D.d操作中有少量水溅出
(3)小华同学用配制的溶液进行中和反应实验,(如图2所示装置),反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
①写出该中和反应的化学方程式______.
②小亮认为小华的结论不准确,他认为除了“两种物质已恰好完全中和”外还有第二种可能性,这种可能性是______.
③请你另外设计一个实验,探究上述烧杯中的溶液是否恰好完全中和.填写下表
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 甲 | 两种物质已恰好完全中和 | ||
| 乙 | 第二种可能性 |
(4)小华同学又用配制的溶液来做碱溶液与酚酞作用的实验.实验时,她发现了一个意外现象:在氢氧化钠溶液中滴入酚酞试液,溶液变成了红色,可是过了一会儿红色就消失了.这是什么原因呢?小华对这种意外现象的成因作了如下猜想:
A.可能是酚酞变质造成的;
B.可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故;
C.可能与氢氧化钠溶液浓度大小有关.
依据所学的化学知识,你认为小华的猜想一定不成立的是______(填字母)
解:(1)氢氧化钠具有强烈的腐蚀性,不能放在纸上称量,应放于玻璃器皿中称量;
(2)导致氢氧化钠溶液溶质的质量分数偏低的因素有溶质偏少、溶剂偏多;
A.a操作中砝码和氢氧化钠放错盘,物码倒置,称量物的质量减小,溶质减少,则溶质的质量分数偏小,正确;
B.b中烧杯用水洗涤后未干燥就使用,造成溶剂的量偏多,则溶质的质量分数偏小,正确;
C.c操作中平视量筒凹液面最低处读数为37.5ml,溶质、溶剂的量正确,溶质的质量分数不变,故错误;
D.d操作中有少量水溅出,不影响溶质的质量分数,故错误;
(3)小华同学用配制的溶液进行中和反应实验,(如图2所示装置),反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
①硫酸和氢氧化钠反应生成硫酸钠和水,反应的化学方程式是2NaOH+H2SO4=Na2SO4+2H2O;
②小亮认为小华的结论不准确,酸碱反应后加入酚酞呈无色,不一定正好完全反应,可能酸过量;
③验证二者恰好完全反应,显中性,可用紫色石蕊试液检验,检验酸是否过量的方法较多,应选择现象明显,操作简便的试剂,可用石蕊试液,滴加碳酸钠,加入锌粒等;
④小华同学在滴入稀硫酸的过程中,观察到有少量气泡出现.产生气泡的原因可能是:部分氢氧化钠与空气中的二氧化碳反应生成碳酸钠,碳酸钠和硫酸反应生成二氧化碳;
(4)氢氧化钠溶液与空气中的二氧化碳反应生成的碳酸钠溶液也显碱性,也能使酚酞变红,所以红色不会消失,故B错误;
开始时,氢氧化钠溶液滴入酚酞试液中溶液变成了红色,所以不是酚酞变质的原因,故A也不正确;
故答案为:(1)称量氢氧化钠时,将氢氧化钠放在纸上称量;
(2)AB;
(3)①2NaOH+H2SO4=Na2SO4+2H2O;
②硫酸过量;
③
④部分氢氧化钠与空气中的二氧化碳反应生成碳酸钠,碳酸钠和硫酸反应生成二氧化碳;
(4)AB.
分析:(1)氢氧化钠具有强烈的腐蚀性,不能放在纸上称量,应放于玻璃器皿中称量;
(2)导致氢氧化钠溶液溶质的质量分数偏低的因素有溶质偏少、溶剂偏多,并结合选项分析解答;
(3)①硫酸和氢氧化钠反应生成硫酸钠和水,据此书写方程式;
②向氢氧化钠溶液中滴加稀硫酸后,加入酚酞溶液不变色,不能说明恰好完全反应,因为当酸过量时酚酞也呈无色;
③探究酸是否过量的方法比较多,可选用指示剂或能与酸反应有明显现象的物质,如碳酸盐,活泼金属等;
(4)可以根据物质性质和实验目的等方面进行分析、判断,从而得出正确的结论.
点评:解答本题时要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,同时要明确酸碱中和的化学方程式,学会检验酸碱的方法,并注意方法的可行性.
(2)导致氢氧化钠溶液溶质的质量分数偏低的因素有溶质偏少、溶剂偏多;
A.a操作中砝码和氢氧化钠放错盘,物码倒置,称量物的质量减小,溶质减少,则溶质的质量分数偏小,正确;
B.b中烧杯用水洗涤后未干燥就使用,造成溶剂的量偏多,则溶质的质量分数偏小,正确;
C.c操作中平视量筒凹液面最低处读数为37.5ml,溶质、溶剂的量正确,溶质的质量分数不变,故错误;
D.d操作中有少量水溅出,不影响溶质的质量分数,故错误;
(3)小华同学用配制的溶液进行中和反应实验,(如图2所示装置),反应后为确定硫酸和氢氧化钠是否刚好完全反应,他取出一定量反应后的溶液于一支试管中,向其中滴入几滴无色酚酞试液,振荡,观察到酚酞试液不变色,于是他得出“两种物质已恰好完全中和”的结论.
①硫酸和氢氧化钠反应生成硫酸钠和水,反应的化学方程式是2NaOH+H2SO4=Na2SO4+2H2O;
②小亮认为小华的结论不准确,酸碱反应后加入酚酞呈无色,不一定正好完全反应,可能酸过量;
③验证二者恰好完全反应,显中性,可用紫色石蕊试液检验,检验酸是否过量的方法较多,应选择现象明显,操作简便的试剂,可用石蕊试液,滴加碳酸钠,加入锌粒等;
④小华同学在滴入稀硫酸的过程中,观察到有少量气泡出现.产生气泡的原因可能是:部分氢氧化钠与空气中的二氧化碳反应生成碳酸钠,碳酸钠和硫酸反应生成二氧化碳;
(4)氢氧化钠溶液与空气中的二氧化碳反应生成的碳酸钠溶液也显碱性,也能使酚酞变红,所以红色不会消失,故B错误;
开始时,氢氧化钠溶液滴入酚酞试液中溶液变成了红色,所以不是酚酞变质的原因,故A也不正确;
故答案为:(1)称量氢氧化钠时,将氢氧化钠放在纸上称量;
(2)AB;
(3)①2NaOH+H2SO4=Na2SO4+2H2O;
②硫酸过量;
③
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| 甲 | 取样,滴加紫色石蕊试液 | 试液不变色 | 两种物质已恰好完全中和 |
| 乙 | 取样,滴加紫色石蕊试液 | 试液变红色 | 第二种可能性 |
(4)AB.
分析:(1)氢氧化钠具有强烈的腐蚀性,不能放在纸上称量,应放于玻璃器皿中称量;
(2)导致氢氧化钠溶液溶质的质量分数偏低的因素有溶质偏少、溶剂偏多,并结合选项分析解答;
(3)①硫酸和氢氧化钠反应生成硫酸钠和水,据此书写方程式;
②向氢氧化钠溶液中滴加稀硫酸后,加入酚酞溶液不变色,不能说明恰好完全反应,因为当酸过量时酚酞也呈无色;
③探究酸是否过量的方法比较多,可选用指示剂或能与酸反应有明显现象的物质,如碳酸盐,活泼金属等;
(4)可以根据物质性质和实验目的等方面进行分析、判断,从而得出正确的结论.
点评:解答本题时要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,同时要明确酸碱中和的化学方程式,学会检验酸碱的方法,并注意方法的可行性.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
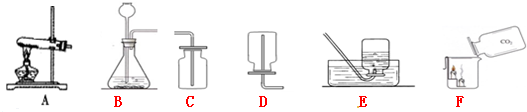
(1)根据下列装置图,回答有关问题:
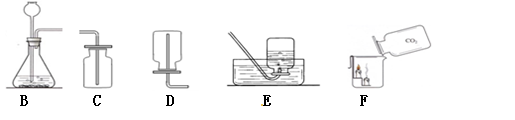
①实验室制取CO2时,选用的发生和收集装置是(填装置字母) 制取CO2的装置还可用于制取 (填一种气体化学式 ),反应的化学方程式为 。
),反应的化学方程式为 。
②如图F所示,向烧杯中倾倒二氧化碳,可观察到的现象是 ,说明二氧化碳具有的性质是 。
③化学兴趣小组查阅资料得知,加热固体碳酸氢钠或固体碳酸氢铵都能产生CO2,
其化学方程式分别是:2NaHCO3△Na2CO3+H2O+CO2↑ NH4HCO3△NH3↑+H2O+CO2↑
某同学采用上述第一个化学反应制取CO2,应该选用的发生装置是______________他不采用上述第二个化学反应制取CO2的理由是________________________________________。
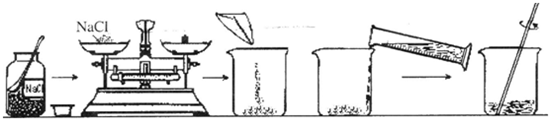
(2)(4分)小华同学配制100g溶质质量分数为20%的NaCl溶液,操作流程如下图:
①小华同学应称取氯化钠的质量是 ;
②指出图中的一处错误: ;
③在用托盘天平称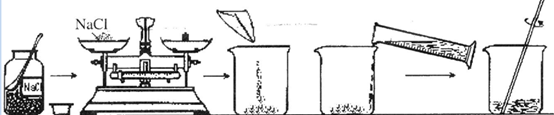 取食盐的过程中,发现指针偏向分度盘右侧,
取食盐的过程中,发现指针偏向分度盘右侧,
他接下来的操作是 (填序号);
④如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能
原因有 (填一种)。

①实验室制取CO2时,选用的发生和收集装置是(填装置字母) 制取CO2的装置还可用于制取 (填一种气体化学式
 ),反应的化学方程式为 。
),反应的化学方程式为 。②如图F所示,向烧杯中倾倒二氧化碳,可观察到的现象是 ,说明二氧化碳具有的性质是 。
③化学兴趣小组查阅资料得知,加热固体碳酸氢钠或固体碳酸氢铵都能产生CO2,
其化学方程式分别是:2NaHCO3△Na2CO3+H2O+CO2↑ NH4HCO3△NH3↑+H2O+CO2↑
某同学采用上述第一个化学反应制取CO2,应该选用的发生装置是______________他不采用上述第二个化学反应制取CO2的理由是________________________________________。
(2)(4分)小华同学配制100g溶质质量分数为20%的NaCl溶液,操作流程如下图:
①小华同学应称取氯化钠的质量是 ;
②指出图中的一处错误: ;
③在用托盘天平称
 取食盐的过程中,发现指针偏向分度盘右侧,
取食盐的过程中,发现指针偏向分度盘右侧,他接下来的操作是 (填序号);
| A.在左盘上减少氯化钠,直至天平平衡 | B.在右盘上减少砝码,直至天平平衡 |
| C.在左盘上继续增加氯化钠,直至天平平衡 | D.移动游码,直至天平平衡 |
原因有 (填一种)。
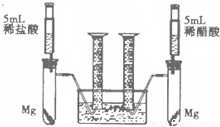
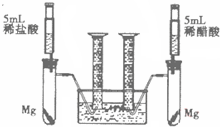 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.

 某校化学兴趣小组对金属活动性顺序等知识进行了研究.
某校化学兴趣小组对金属活动性顺序等知识进行了研究.