题目内容
化学小组的同学在学习了酸碱中和反应后,设计了一个能观察到明显现象的实验,说明氢氧化钠溶液与稀盐酸确实发生了反应.请帮助他们填写下列实验报告.| 实验步骤 | 实验现象 | 实验结论 |
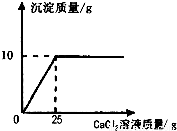
【答案】分析:根据酚酞试液遇碱性溶液变红以及遇中性或酸性溶液不变色,借助酚酞试液从而判断氢氧化钠溶液与稀盐酸确实发生了反应;碳酸钠溶液和氯化钙溶液反应生成碳酸钙白色沉淀,由沉淀的质量求出碳酸钠的质量,进而求出氢氧化钠的质量即可进行解答.
解答:解:酚酞试液遇碱性溶液变红,而遇中性或酸性溶液不变色,借助酚酞试液从而判断氢氧化钠溶液与稀盐酸确实发生了反应.
故答案为:
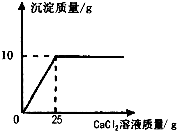
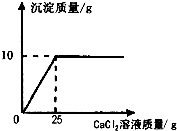
设样品中碳酸钠的质量为x.由图可知碳酸钙的质量为10g.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
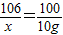
x=10.6g
该样品中氢氧化钠的质量分数=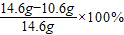 =27.4%
=27.4%
答:该样品中氢氧化钠的质量分数为27.4%.
点评:本题考查了酸碱中和反应以及物质的性质,完成此题,可以依据已有的知识进行,要求同学们加强对基础知识的储备,以便灵活应用.
解答:解:酚酞试液遇碱性溶液变红,而遇中性或酸性溶液不变色,借助酚酞试液从而判断氢氧化钠溶液与稀盐酸确实发生了反应.
故答案为:
| 实验步骤 | 实验现象 | 实验结论 |
| 1、取少量氢氧化钠溶液于小烧杯中,滴加几滴无色的酚酞试液 2、向上述溶液中逐滴加入稀盐酸,并振荡 | 1、溶液变红色 2、溶液由红色变为无色 | 1、碱溶液能使酚酞试液变红 2、氢氧化钠溶液与稀盐酸确实发生了反应 |
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
x 10g
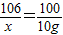
x=10.6g
该样品中氢氧化钠的质量分数=
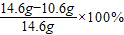 =27.4%
=27.4% 答:该样品中氢氧化钠的质量分数为27.4%.
点评:本题考查了酸碱中和反应以及物质的性质,完成此题,可以依据已有的知识进行,要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
 化学小组的同学在学习了酸碱中和反应后,设计了一个能观察到明显现象的实验,说明氢氧化钠溶液与稀盐酸确实发生了反应.请帮助他们填写下列实验报告.
化学小组的同学在学习了酸碱中和反应后,设计了一个能观察到明显现象的实验,说明氢氧化钠溶液与稀盐酸确实发生了反应.请帮助他们填写下列实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
某化学小组的同学在学习《奇妙的二氧化碳》时,设计了如下图实验:

| 实验步骤及操作 | 实验现象 |
| ① 将注射器1中的水推入充有CO2的三颈烧瓶中,振荡。 | 气球略微鼓起 |
| ②
| 澄清石灰水变浑浊 |
| ③ 将注射器2中的溶液推入三颈烧瓶中 | 溶液中 ,气球变瘪。 |
问题讨论:
⑴ 步骤①中现象产生的原因是 ,此实验说明,在密闭的体系内,气压变小的原因是 。 试写出你学过的实验中,也是运用此原理的实验 。结合“热胀冷缩”原理,气压变小的另一原因是 。
⑵ 填写②中的操作。
⑶ 若将步骤①中的水改为相同体积的浓氢氧化钠溶液,再进行步骤②时,发现石灰水未变浑浊,此实验说明 。结合问题⑴试比较:推入氢氧化钠溶液时气球的大小 推入同体积水时的气球的大小(填“大于”或“小于”或“等于”)。
⑷ ③中现象原因(用符号表达式表示) 。
 (2007?丰台区一模)化学小组的同学在学习了酸碱中和反应后,设计了一个能观察到明显现象的实验,说明氢氧化钠溶液与稀盐酸确实发生了反应.请帮助他们填写下列实验报告.
(2007?丰台区一模)化学小组的同学在学习了酸碱中和反应后,设计了一个能观察到明显现象的实验,说明氢氧化钠溶液与稀盐酸确实发生了反应.请帮助他们填写下列实验报告.