题目内容
【题目】食盐的主要成分是NaCl, 食盐中因含有MgCl2而容易潮解,现取40g含MgCl2的食盐样品做如下实验,已知:MgCl2+2NaOH=Mg(OH)2↓+2NaCl请根据图中实验及数据进行计算:
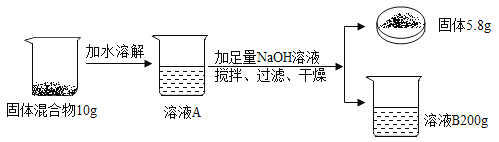
(1)MgCl2中镁元素和氯元素的质量比为____。
(2)样品中氯化钠的质量分数(写出计算过程)。
(3)计算溶液B中的氯化钠的质量分数(写出计算过程)。
【答案】(1)24:71
(2)5%(详见解析)
(3)6.1%(详见解析)
【解析】
(1)MgCl2中镁元素和氯元素的质量比为24:(35.5×2)=24:71。
(2)设样品中氯化镁质量为x,反应生成氯化钠质量为y。
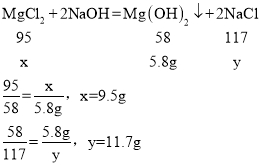
故氯化钠的质量分数为:![]()
(3)B中的氯化钠的质量:10g-9.5g+11.7g=12.2g;
故B中的氯化钠的质量分数:![]() 。
。

练习册系列答案
相关题目