题目内容
【题目】下表为元素周期表中部分元素的相关信息,请利用下表回答问题:
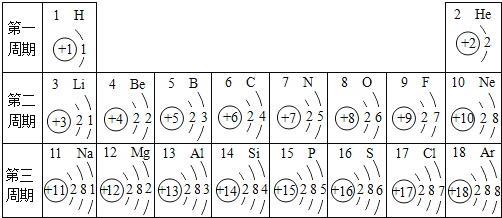
(1)原子序数为16的元素属于_____________(填“金属”或“非金属”)元素。表中与该元素化学性质相似的元素是_____________。(填元素名称)
(2)M2—与Ne 核外电子排布相同,已知M 元素的相对原子质量为a,则M 元素原子核内的中子数为_____________。
【答案】非金属 氧 a-8
【解析】
(1)16号元素是硫,硫元素带石字旁,属于非金属元素;最外层电子数决定元素的化学性质,最外层电子数相同的元素,化学性质相似,硫元素原子最外层电子数为6,氧元素原子最外层电子数为6,因此硫、氧元素的化学性质相似;故填:氧;
(2)Ne为10号元素,原子序数=原子的核外电子数=10,M2-是由M原子得到2个电子形成的,其核外有10个电子,则M核外有8个电子,核电荷数为8,是氧元素,因为相对原子质量=质子数+中子数,所以氧原子核内的中子数为:a-8。故填:a-8。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目