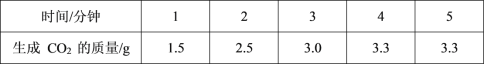题目内容
【题目】用NA表示阿伏伽德罗常数的值。下列叙述中正确的是( )
A. 分子总数为NA 的NO2和CO2混合气体中含有的氧原子数为4NA
B. 常温常压下,92gNO2和N2O4混合气体中含有的原子数为6NA
C. 1mol SO3中含有的分子数目为4NA
D. 含有3.01×1023个原子的氮气中,N2的分子数为0.5NA
【答案】B
【解析】
A. 分子总数为 NA 的 NO2 和 CO2 混合气体中含有的氧原子数为2NA,因为不管是NO2还是CO2一个分子只有2个氧原子,而分子总数是NA个,故氧原子数为2NA,故不符合题意;
B. 常温常压下,92gNO2 和 N2O4 混合气体中含有的原子数为 6NA,说法正确,因为NO2 和 N2O4 的N、O原子个数比为1:2,其摩尔质量为![]() ,其物质的量为
,其物质的量为![]() ,1mol有3NA个原子,2mol有6NA个原子,故符合题意;
,1mol有3NA个原子,2mol有6NA个原子,故符合题意;
C. 1molSO3 中含有的分子数目为NA,含有的原子数为4NA。故不符合题意;
D. 含有 3.01×1023 个原子的氮气,有0.25mol的氮气,N2 的分子数为 0.25NA。故不符合题意;

 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
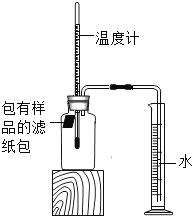
三新快车金牌周周练系列答案【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。