题目内容
【题目】根据实验装置图,回答问题。
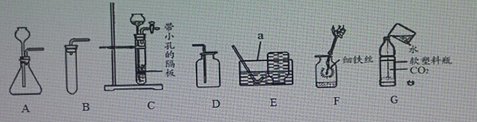
① 仪器a的名称是___________________。
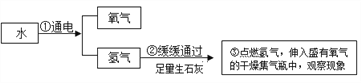
② 用过氧化氢溶液和二氧化锰的混合物制取氧气。
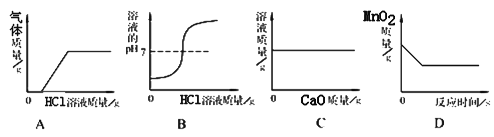
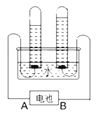
(Ⅰ)请你在“A”、“B”两套装置中选择其中一套作为发生装置,并说明选择的理由。____________。
(Ⅱ)如用D装置收集O2,检验O2是否收集满的方法是__________________。
(Ⅲ)二氧化锰的作用是_______;反应结束后,要回收混合物中的MnO2,实验操作是_______。
(Ⅳ)探究溶质质量分数对过氧化氢分解速率的影响:分别取10mL 5%、15%、30%的过氧
化氢溶液三份,测定收集到100mL氧气所用的时间(其它实验条件均相同),记录如下:
实验编号 | 1 | 2 | 3 |
过氧化氢溶液的溶质质量分数 | 5% | 15% | 30% |
所用时间(秒) | 205 | 25 | 3 |
实验结论 | ___________________________ | ||
(Ⅴ)用收集的氧气完成图F铁丝燃烧的实验,为使铁丝在氧气中持续剧烈燃烧,把光亮的细铁丝盘成螺旋状,_________,缓慢插入集气瓶中,观察到持续剧烈燃烧;该反应的化学方程为_______。
③ 用大理石和稀盐酸反应制取二氧化碳。
(Ⅰ)制取二氧化碳时,能随时控制反应的发生和停止,则选择的发生装置和收集装置是______(写序号)。
(Ⅱ)反应结束后,生成了0.2mol二氧化碳,求稀盐酸中参与反应的HCl的质量。__________(根据化学方程式列式计算)。
(Ⅲ)如图G向装满CO2 的软塑料瓶注入约1/3体积的水,立即旋紧瓶盖,振荡,再在软塑料瓶中滴入紫色石蕊试液,观察到的现象是___________。
【答案】 水槽 A,便于添加液体药品(或能制得较多气体)【或B,装置简单(或节约药品)】 将一根带火星的木条放在集气瓶口,木条复燃,证明收集满 加快反应速度(或催化作用) 过滤 相同条件下,过氧化氢溶液溶质质量分数越大,过氧化氢分解速率越快 下端系一根火柴,点燃火柴,待火柴快燃尽时 3Fe + 2O2 ![]() Fe3O4 C D 14.6g 软塑料瓶变瘪,试液从紫色变为红色
Fe3O4 C D 14.6g 软塑料瓶变瘪,试液从紫色变为红色
【解析】①根据常见仪器解答;②(Ⅰ)根据用过氧化氢溶液和二氧化锰是固体和液体在常温下反应及装置的特点分析解答;(Ⅱ)根据用向上排空气法收集氧气验满的方法解答;(Ⅲ)根据二氧化锰在过氧化氢的分解过程中起催化作用解答;根据分离固液混合解答;(Ⅳ)根据表中数据分析解答;(Ⅴ)根据铁丝在氧气中燃烧的实验操作步骤、注意事项及反应原理解答;③(Ⅰ)根据实验要求及装置的特点选择发生装置,根据二氧化碳的密度及溶解性选择收集装置;(Ⅱ)根据生成二氧化碳的质量求解HCl的质量;(Ⅲ)根据二氧化碳与水反应生成碳酸,碳酸使紫色石蕊溶液变红且瓶内气压降低解答。①仪器a的名称是水槽;②(Ⅰ)用过氧化氢溶液和二氧化锰的混合物制取氧气选择A装置作为发生装置,理由是便于添加液体药品等(或B,装置简单等);(Ⅱ)用D装置收集O2,是用向上排空气法收集O2,检验O2是否收集满的方法是将一根带火星的木条放在集气瓶口,木条复燃,证明收集满;(Ⅲ)二氧化锰的作用是催化作用;反应结束后,要回收混合物中的MnO2,实验操作是过滤;(Ⅳ)由表中数据可知,相同条件下,过氧化氢溶液溶质质量分数越大,过氧化氢分解速率越快;(Ⅴ)用收集的氧气完成图F铁丝燃烧的实验,为使铁丝在氧气中持续剧烈燃烧,把光亮的细铁丝盘成螺旋状,下端系一根火柴,点燃火柴,待火柴快燃尽时,缓慢插入集气瓶中,观察到持续剧烈燃烧;该反应的化学方程式为3Fe+2O2![]() Fe3O4;③(Ⅰ)制取二氧化碳时,能随时控制反应的发生和停止,应选择C装置,当打开止水夹时,长颈漏斗中的稀盐酸与大理石接触,反应开始,当关闭止水夹时,装置内气压增大,将稀盐酸压回到长颈漏斗中,使稀盐酸与塑料隔板分离,反应停止,由于二氧化碳的密度比空气大且能溶于水,故应选择D做为收集装置;
Fe3O4;③(Ⅰ)制取二氧化碳时,能随时控制反应的发生和停止,应选择C装置,当打开止水夹时,长颈漏斗中的稀盐酸与大理石接触,反应开始,当关闭止水夹时,装置内气压增大,将稀盐酸压回到长颈漏斗中,使稀盐酸与塑料隔板分离,反应停止,由于二氧化碳的密度比空气大且能溶于水,故应选择D做为收集装置;
(Ⅱ)稀盐酸中参与反应的HCl的质量为x。
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 1mol
x 0.2mol
![]()
x=14.6g
(Ⅲ)如图G向装满CO2 的软塑料瓶注入约1/3体积的水,立即旋紧瓶盖,振荡,再在软塑料瓶中滴入紫色石蕊试液,观察到的现象是软塑料瓶变瘪,试液从紫色变为红色。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案