题目内容
【题目】被誉为“中国天眼”的FAST,是目前世界上最大口径、最灵敏的射电望远镜。其主体部分由铝合金反射镜面与支撑它的角钢(含有锰(Mn))塔架组成。
(1)选择角钢而不用纯铁做塔架的原因是___。
(2)常用氧炔焰焊接角钢塔架。为了使焊接更牢固,燃烧时需要调节乙炔与氧气的体积比为___。焊接前需要用稀盐酸除铁锈,反应的化学方程式为___。
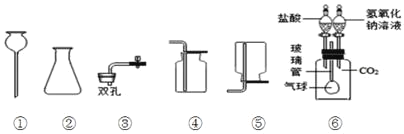
(3)为探究Fe、Cu、Mn三种金属的活动性,进行了如图1所示的实验:

若实验③中观察到了明显的现象。通过以上实验,判断三种金属的活动性由强到弱的顺序为___。实验①~④中,不需要做的实验是___(填序号)。
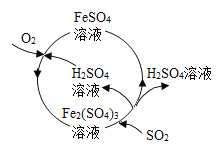
(4)电望远镜生产需要线路板。工业上常用氯化铁溶液腐蚀铜的原理生产印刷线路板。如图是印刷线路板的生产及废液的处理过程。试回答

①步骤②中发生了两个反应:2FeCl3+Fe═3FeCl2和___。
②操作I、Ⅱ的名称是___操作Ⅱ所得滤液中的溶质为___。
③步骤①中参加反应的氯化铁与铜的质量比为___。
【答案】钢的硬度大 1:5 Fe2O3+6HCl=2FeCl3+3H2O 锰>铁>铜 ④ CuCl2+Fe═FeCl2+Cu 过滤 氯化亚铁 325:128
【解析】
(1)选择角钢而不用纯铁作塔架是因为钢的硬度大。故填:钢的硬度大;
(2)根据2C2H2+5O2![]() 4CO2+2H2O可知,乙炔与氧气恰好完全反应时的体积比为1:5.铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.故填:1:5;Fe2O3+6HCl=2FeCl3+3H2O;
4CO2+2H2O可知,乙炔与氧气恰好完全反应时的体积比为1:5.铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.故填:1:5;Fe2O3+6HCl=2FeCl3+3H2O;
(3)若实验③中观察到了明显的现象,说明了锰>铁,根据金属活动性顺序表可知铁>铜,则三者的活动性由强到弱的顺序为锰>铁>铜。实验①②说明了铁>铜,实验③说明锰>铁,实验④说明锰>铜,实验①②③即可证明三者的活动性强弱,不需要做实验④.故填:锰>铁>铜,④;
(4)①步骤②中铁能与氯化铜反应生成氯化亚铁和铜,反应的化学方程式为CuCl2+Fe=FeCl2+Cu.故填:CuCl2+Fe=FeCl2+Cu;
②通过步骤ⅠⅡ分离得到滤液和滤渣,进行了固液分离,说明该操作是过滤;步骤②过量的铁粉与氯化铜、氯化铁反应后,所得滤液中的溶质是氯化亚铁,滤渣的成分是生成的铜和剩余铁粉,滤渣加入适量盐酸,铜不反应,铁与盐酸反应生成氯化亚铁和氢气,所得滤液的成分还是氯化亚铁。故填:过滤;氯化亚铁;
③根据2FeCl3+Cu=2FeCl2+CuCl2中各物质之间的质量比可知,参加反应的氯化铁和铜的质量比为325:128.故填:325:128。