题目内容
【题目】含硫煤燃烧会产生大气污染。为防治该污染,某工厂设计的新的治污方法不仅吸收了 SO2, 同时还得到了某种化工产品。该工艺流程如图所示,下列叙述不正确的是
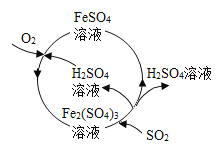
A. 该流程中可得到化工产品 H2SO4
B. 图中 FeSO4 → Fe2(SO4)3 的反应类型是复分解反应
C. 该流程中化合价发生改变的元素为 Fe、S 和 O
D. 图中吸收 SO2 的化学反应方程式为:Fe2(SO4)3 + SO2 + 2H2O == 2FeSO4 + 2H2SO4
【答案】B
【解析】
A、工艺流程图可以看出,转化过程中吸收了氧气和二氧化硫,排出了硫酸,所以该流程中可得到化工产品硫酸,故A正确;B、复分解反应过程中,元素的化合价不变,所以图中FeSO4→Fe2(SO4)3的反应类型不属于复分解反应,故B错误;C、该流程中化合价发生改变的元素为Fe、S和O,故C正确;D、硫酸铁、水和二氧化硫反应生成硫酸亚铁和硫酸,所以图中吸收SO2的化学反应方程式为:Fe2(SO4)3+SO2+2H2O=2FeSO4+2H2SO4,故D正确。故选B。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】某同学对下表中的溶解度数据分析后,得出的结论错误的是( )
温度/℃ | 0 | 20 | 40 | 60 |
氢氧化钙的溶解度/g | 0.18 | 0.16 | 0.14 | 0.11 |
硝酸钾的溶解度/g | 13.3 | 31.6 | 61.9 | 110 |
氯化钠的溶解度/g | 35.7 | 36 | 36.6 | 37.2 |
A. 升温可将20℃时不饱和的Ca(OH)2溶液变为饱和溶液
B. 60℃,饱和KNO3溶液的质量分数约为52.4%
C. 温度变化对NaCl的溶解度影响较小
D. NaCl的溶解度大于KNO3的溶解度
【题目】超市出现了一种含“污渍爆炸盐”的新产品(如图),能清除衣服上难以清洗的汗 渍、果汁渍。它的特殊的名称让小明对它产生了探究的兴趣。

(1)小明在超市的___区域购买了此产品。
(2)阅读产品标签:“污渍爆炸盐”是一种衣物助洗剂,主要成分是过碳酸钠,能在瞬间去除洗衣液难以除去的多种顽固污 渍……,本产品不伤衣物,无磷是它的一大优点。含磷洗涤剂对环 境的危害是______。
(3)查阅资料:过碳酸钠(Na2CO4)是白色结晶颗粒,溶于水 会产生碳酸盐和其它化合物。
(4)合理猜想其它化合物为:
i. NaOH;ii. H2O2;iii. NaOH 和 H2O2;小明做出以上猜想的理论依据是___。
(5)实验设计:探究“污渍爆炸盐”水溶液的成分,完成下列表格。 已知:Mg(OH)2 是难溶于水的白色固体。
实验步骤 | 实验现象 | 实验结论 |
步骤 1:取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水,充分搅拌。 | 固体完全溶解,形成无色溶液 | |
步骤 2:取少量步骤 1 形成的溶液于试管中,再加 入___ , 振荡,静置。 | 白色沉淀 | 含有 Na2CO3 |
步骤 3:取少量步骤 2 试管中的上层清液于另一支 试管中,再滴加少量 MgCl2 溶液,振荡。 | 无明显现象 | ___ |
步骤 4:另取一支试管,加入少量步骤 1 形成的溶 液,再加入__ , 将带火星木条伸入试管中。 | ___ | 含有 H2O2 |
(6)实验结论:猜想__ 正确。写出过碳酸钠与水反应的化学方程式:____ 。
【题目】下图是我们所用课本中的一张,根据图示信息回答下列问题:

(1)该元素的核内质子数为________
(2)该原子的结构示意图为________
(3)若该元素元素的元素符号用A表示,则它与氧元素形成化合物的化学式为________
(4)下列对原子构成的理解错误的是_________(填字母)。
A.原子整体不显电性 |
B.原子核比原子小得多 |
C.原子核是不可分割的实心球体 |
D.原子质量主要集中在原子核上 |
(5)在元素周期表中,第二周期的八种元素中________相同。