题目内容
【题目】在化学反应中,只要物质所含元素的化合价发生了变化的反应就是氧化还原反应。例如:2Na+C12=2NaCl,反应前后,Na元素、Cl元素的化合价分别发生了变化,该反应是氧化还原反应。
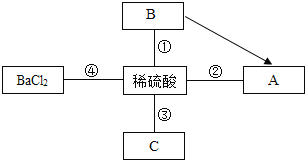
(1)根据化合价是否发生变化分析,下列反应(部分反应条件略去)中属于氧化还原反应的是_____(填序号)。
①C+O2=CO2 ②CaO+H2O=Ca(OH)2 ③CaCO3=CaO+CO2↑
④2H2O2=2H2O+O2↑ ⑤CO+CuO=Cu+CO2 ⑥HCl+NaOH=NaCl+H2O
(2)通过进一步定量分析上述氧化还原反应的化合价变化发现:氧化还原反应中元素化合价升高总数_____(填“大于”、“等于”或“小于”)元素化合价降低总数。
(3)含有高价态元素的化合物,通常具有氧化性,如在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁。该反应的还原剂是_____。
(4)柠檬果汁中含有维生素C(C6H8O6)是还原剂,它能被I2氧化生成C6H6O6.该反应的化学方程式为_____。
【答案】①④⑤ 等于 Cu ![]()
【解析】
(1)①碳元素的化合价从0升高到+4价,氧元素的化合价从0降低到﹣2价,有化合价的变化,属于氧化还原反应,故正确;
②反应中Ca、H、O三种元素的化合价都没有变化,则不属于氧化还原反应,故错误;
③反应中Ca、C、O三种元素的化合价都没有变化,则不属于氧化还原反应,故错误;
④氧元素的化合价从﹣1价变为﹣2价和0价,有化合价的变化,属于氧化还原反应,故正确;
⑤反应中,碳元素由+2价升高为+4价,铜元素显+2价降低为0价,故正确;
⑥反应中Cl、H、Na、O四种元素的化合价都没有变化,则不属于氧化还原反应,故错误。
故选:①④⑤;
(2)通过进一步定量分析上述氧化还原反应的化合价变化发现:氧化还原反应中元素化合价升高总数等于元素化合价降低总数。故填:等于;
(3)在氯化铁溶液中,氯化铁能将单质铜氧化成氯化铜,自身被还原成氯化亚铁,铁元素由+3价降低为+2价,所以氯化铁是氧化剂,铜元素由0价升高为+2价,铜属于还原剂;故填:Cu;
(4)维生素C(C6H8O6)是还原剂,它能被I2氧化生成C6H6O6,同时生成碘化氢;故填:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】请从A或B中任选一个作答,若均作答,按A计分。
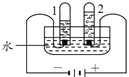
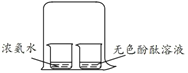
A探究水的组成 | B探究分子的性质 |
|
|
(1)检验试管2中生成的气体,可用_____。 (2)该实验的结论为____。 | (1)实验中观察到的现象为____。 (2)该实验的结论为____。 |