题目内容
(10盐城17.)(14分)(1)根据下列装置图回答问题。

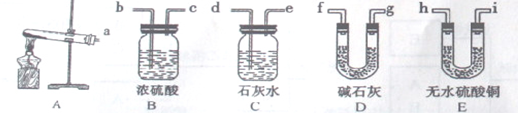
①写出图中标有小写字母的仪器的名称:
a ▲ b ▲ 。
②若用氯酸钾制取氧气,就选用的发生装置是 ▲ (填字母序号)。
用D装置收集氧气,停止加热时,必须先 ▲ ,后 ▲ 。
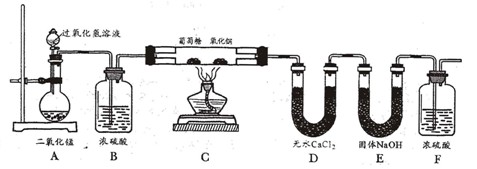
③写出实验室制取二氧化碳的化学方程式 ▲ ,选用图中和(填字母序号)组装一套制取二氧化碳的装置。检验二氧化碳集满的方法是 ▲ 。
(2)为鉴别失去标签的五瓶溶液:稀盐酸、碳酸钠溶液、硝酸钡溶液、硫酸钠溶液和硝酸钠溶液,将其任意编号,进行两两混合,其部分实验现象见下表:
①写出有关的化学式:C ▲ ,D ▲ ;
②写出A与B反应的化学方程式: ▲ 。

①写出图中标有小写字母的仪器的名称:
a ▲ b ▲ 。
②若用氯酸钾制取氧气,就选用的发生装置是 ▲ (填字母序号)。
用D装置收集氧气,停止加热时,必须先 ▲ ,后 ▲ 。
③写出实验室制取二氧化碳的化学方程式 ▲ ,选用图中和(填字母序号)组装一套制取二氧化碳的装置。检验二氧化碳集满的方法是 ▲ 。
(2)为鉴别失去标签的五瓶溶液:稀盐酸、碳酸钠溶液、硝酸钡溶液、硫酸钠溶液和硝酸钠溶液,将其任意编号,进行两两混合,其部分实验现象见下表:
| 实验 | A+D | A+B | B+C |
| 现象 | 产生气体 | 产生沉淀 | 产生沉淀 |
①写出有关的化学式:C ▲ ,D ▲ ;
②写出A与B反应的化学方程式: ▲ 。
(14分)方程式每空2分,其余每空1分
(1)①a长颈漏斗 b 集气瓶(错别字,该空不给分)
②A,将导气管移出水面,后熄灭酒精灯,CaCO3+2HCl=CaCl2+H2O+CO2↑(化学式书写全部正确,未配平、气体符号漏写或错写的,累计扣1分)
③B和C,将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满。
(2)①C: Na2SO4 D:HCl(写物质名称正确得1分);Na2CO3+ Ba(NO3)2=Ba CO3↓+ 2Na NO3(化学式书写全部正确,未配平、沉淀符号漏写或错写的,累计扣1分)
(1)①a长颈漏斗 b 集气瓶(错别字,该空不给分)
②A,将导气管移出水面,后熄灭酒精灯,CaCO3+2HCl=CaCl2+H2O+CO2↑(化学式书写全部正确,未配平、气体符号漏写或错写的,累计扣1分)
③B和C,将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满。
(2)①C: Na2SO4 D:HCl(写物质名称正确得1分);Na2CO3+ Ba(NO3)2=Ba CO3↓+ 2Na NO3(化学式书写全部正确,未配平、沉淀符号漏写或错写的,累计扣1分)
(1)图中是a长颈漏斗,b是集气瓶.
故答案为:长颈漏斗、集气瓶;
②用氯酸钾制取氧气,是固固加热反应,所以我们可选用A作为发生装置;实验完毕后,为防止水进入试管,要先将导气管移出水面,再熄灭酒精灯.
故答案为:A、将导气管移出水面、后熄灭酒精灯;
③实验室常用大理石与石灰石反应制取二氧化碳,化学反应式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;因此反应是固液不加热反应,所以可以用B作为发生装置;因二氧化碳密度大于空气的密度,并不易溶于水,我们可选用C向上排气法收集气体;因二氧化碳不支持燃烧,验满时可将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑、B、C、将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满;
(2)①五种溶液中只有HCl溶液和Na2CO3溶液混合生成二氧化碳;HCl溶液不能再与其他三种五种反应,所以A是Na2CO3溶液,D是HCl溶液;又知A+B产生沉淀,与A(Na2CO3溶液)反应生成沉淀的物质只有Ba(NO3)2溶液,故B是Ba(NO3)2溶液;又知B【Ba(NO3)2溶液】与C反应生成沉淀,剩余的两种物质中与B反应生成沉淀的物质是Na2SO4溶液,所以C是Na2SO4溶液.
故答案为:C:Na2SO4、D:HCl;
②根据反应物是Na2CO3溶液和Ba(NO3)2溶液,可以确定化学反应式是:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3.
故答案为:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3.
点评:此题考查的是几种常见物质的推断,要解决此类题目,就要熟悉常见物质间的化学反应及有关的实验现象,另外关键是找准解题的突破口,突破口找准了,完成此类题目就势如破竹,所以还要求同学们加强知识的积累.
故答案为:长颈漏斗、集气瓶;
②用氯酸钾制取氧气,是固固加热反应,所以我们可选用A作为发生装置;实验完毕后,为防止水进入试管,要先将导气管移出水面,再熄灭酒精灯.
故答案为:A、将导气管移出水面、后熄灭酒精灯;
③实验室常用大理石与石灰石反应制取二氧化碳,化学反应式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;因此反应是固液不加热反应,所以可以用B作为发生装置;因二氧化碳密度大于空气的密度,并不易溶于水,我们可选用C向上排气法收集气体;因二氧化碳不支持燃烧,验满时可将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑、B、C、将燃着的木条放在集气瓶口,火焰立即熄灭,说明已满;
(2)①五种溶液中只有HCl溶液和Na2CO3溶液混合生成二氧化碳;HCl溶液不能再与其他三种五种反应,所以A是Na2CO3溶液,D是HCl溶液;又知A+B产生沉淀,与A(Na2CO3溶液)反应生成沉淀的物质只有Ba(NO3)2溶液,故B是Ba(NO3)2溶液;又知B【Ba(NO3)2溶液】与C反应生成沉淀,剩余的两种物质中与B反应生成沉淀的物质是Na2SO4溶液,所以C是Na2SO4溶液.
故答案为:C:Na2SO4、D:HCl;
②根据反应物是Na2CO3溶液和Ba(NO3)2溶液,可以确定化学反应式是:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3.
故答案为:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3.
点评:此题考查的是几种常见物质的推断,要解决此类题目,就要熟悉常见物质间的化学反应及有关的实验现象,另外关键是找准解题的突破口,突破口找准了,完成此类题目就势如破竹,所以还要求同学们加强知识的积累.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
 Cu+H2O,某同学为了验证氢气还原氧化铜的产物,设计了如下由A、B、C三部分组成的实验装置。
Cu+H2O,某同学为了验证氢气还原氧化铜的产物,设计了如下由A、B、C三部分组成的实验装置。