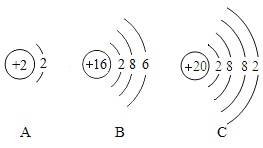
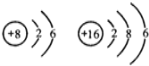
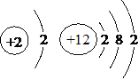题目内容
【题目】今年,我们偃师市的好多农村也通上了天然气,某化学兴趣小组的同学对天然气(主要成分是甲烷)燃烧的产物产生了兴趣,设计实验探究:
(提出问题)天然气燃烧后生成哪些物质?
(查阅资料)①含碳元素的物质完全燃烧生成CO2,不完全燃统生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人缺氧中毒。
(猜想与假设)猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
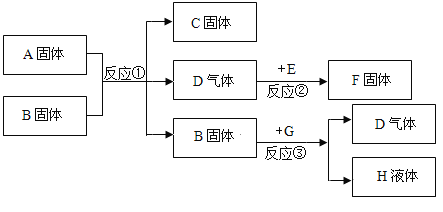
(实验探究)将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
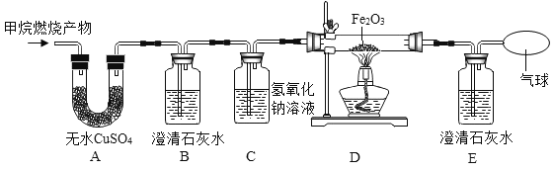
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想_____成立。
(2)实验过程中B装置的作用是_____;该反应的化学方程式是_____。
(3)D装置中发生反应的化学方程式是_____。
(4)实验过程中用纯净O2,而不用空气的原因是_____。
(5)实验过程中B、C装置的顺序不能颠倒,原因是_____。
(6)(反思与交流)日常生活中,使用含碳燃料一定要注意通风,防止_____中毒。
(7)实验所需纯净的O2,可用氯酸钾制备,请计算制备4.85gO2需要多少氯酸钾?_____(写出计算过程,计算结果保留一位小数)
【答案】三 检验是否含有二氧化碳 ![]()
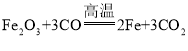 空气含有二氧化碳和水蒸气,会影响燃烧产物的验证; )如果实验过程中将B、C装置的顺序颠倒,二氧化碳会被氢氧化钠完全吸收,再通过澄清石灰水,不会出现浑浊现象,无法判断产物中是否含有二氧化碳 CO 设制备4.85gO2需要x克氯酸钾
空气含有二氧化碳和水蒸气,会影响燃烧产物的验证; )如果实验过程中将B、C装置的顺序颠倒,二氧化碳会被氢氧化钠完全吸收,再通过澄清石灰水,不会出现浑浊现象,无法判断产物中是否含有二氧化碳 CO 设制备4.85gO2需要x克氯酸钾
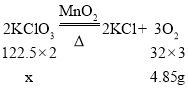
![]()
x=12.4g
故制备4.85gO2需要12.4克氯酸钾。
【解析】
(1)实验过程中观察到A中白色粉末变为蓝色,A中为无水硫酸铜,无水硫酸铜遇水变蓝,说明气体中含有水蒸气,B中澄清石灰水变浑浊,说明气体中含有二氧化碳,E中澄清石灰水变浑浊,说明D中产生了二氧化碳,D中红棕色粉末变成黑色,三氧化二铁被CO还原生成了铁,说明气体中含有一氧化碳,故猜想三成立;
(2)B装置的作用是检验是否含有二氧化碳,因为二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,该反应的化学方程式是:![]() ;
;
(3)D装置中发生反应的化学方程式是: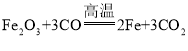 ;
;
(4)实验过程中用纯净O2,而不用空气,是因为空气含有二氧化碳和水蒸气,会影响燃烧产物的验证;
(5)如果实验过程中将B、C装置的顺序颠倒,二氧化碳会被氢氧化钠完全吸收,再通过澄清石灰水,不会出现浑浊现象,无法判断产物中是否含有二氧化碳;
(6)日常生活中,使用含碳燃料,如果含碳燃料燃烧不充分,就会生成一氧化碳,因此使用含碳燃料一定要注意通风,防止CO中毒;
(7)设制备4.85gO2需要x克氯酸钾
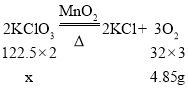
![]()
x=12.4g
故制备4.85gO2需要12.4克氯酸钾。

 备战中考寒假系列答案
备战中考寒假系列答案