题目内容
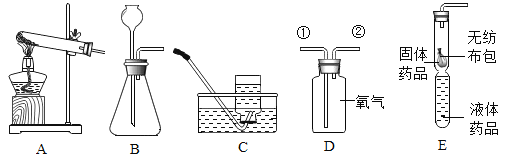
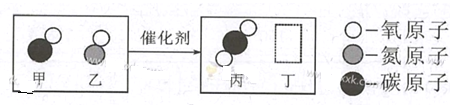
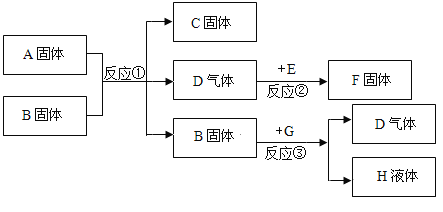
【题目】A,B,C,D,E,F,G都是初中化学中常见物质,A是白色固体,B和F是黑色固体,G和H是无色液体,E在D中燃烧的现象非常剧烈,火星四射;B在反应③中作催化剂;它们之间的转换关系如图所示:
(1)写出下列物质的名称:E_____;G_______;
(2)写出物质F的符号_______;
(3)写出上述①反应的文字表达式________,基本反应类型是_________。
(4)写出上述③反应的符号表达式________,物质B在该反应中_______都不变。
【答案】铁 过氧化氢 Fe3O4 氯酸钾![]() 氯化钾+氧气 分解反应 H2O2
氯化钾+氧气 分解反应 H2O2![]() H2O+O2 质量和化学性质
H2O+O2 质量和化学性质
【解析】
A是白色固体,B和F是黑色固体,G和H是无色液体,E在D中燃烧的现象非常剧烈,火星四射,则D为氧气,E为铁,F为生成的四氧化三铁;氯酸钾是一种白色固体,在二氧化锰的催化作用下生成氯化钾和氧气,则A为氯酸钾,B为二氧化锰,C为生成的氯化钾;B在反应③中作催化剂,过氧化氢在二氧化锰的催化作用下生成水和氧气,则G为过氧化氢溶液,H为水。
(1)由分析可知:E是铁;G是过氧化氢。
(2)由分析可知,F是四氧化三铁,符号为Fe3O4。
(3)上述①反应是氯酸钾和二氧化锰加热生成氯化钾和氧气,反应的文字表达式为氯酸钾![]() 氯化钾+氧气,反应符合一变多,故基本反应类型是分解反应。
氯化钾+氧气,反应符合一变多,故基本反应类型是分解反应。
(4)上述③反应是过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的符号表达式为H2O2![]() H2O+O2,物质B(二氧化锰)是该反应的催化剂,在该反应中质量和化学性质都不变。
H2O+O2,物质B(二氧化锰)是该反应的催化剂,在该反应中质量和化学性质都不变。

 期末集结号系列答案
期末集结号系列答案【题目】铜丝在空气中加热生成氧化铜,思然同学采用了下图所示装置测定空气中的氧气含量,在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,使铜丝和氧气反应,并交替推动两个注射器活塞,然后停止加热,将剩余气体全部推至一个注射器内,观察密闭系统内空气体积变化。

(1)在加热过程中,交替推动两个注射器活塞的目的_______。
(2)写出该实验中反应的文字表达式_______。
(3)实验中思然同学测得实验结果如下
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
25mL | 21mL |
上述表格中数据计算出空气中氧气的体积分数为_____%,造成实验误差的原因可能是_____(填序号)
①推动两个注射器活塞的速度过快;②读数时没有冷却至室温;③铜丝量太少
(4)上述实验中常用加热铜丝或铜粉与氧气反应,而不选择铜块或铜片,这样做的目的是通过_____来加快反应速率。