题目内容
【题目】实验室常用石灰石和稀盐酸制取二氧化碳。某学生取15g的石灰石和足量的稀盐酸于烧杯中,待其充分反应后,称得烧杯的总质量比原来少了4.4g。请回答以下问题:
(1)生成的二氧化碳质量为______g。
(2)求该石灰石中碳酸钙的质量分数。______(反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)
【答案】4.4 66.7%
【解析】
(1)由质量守恒定律,烧杯内减少的质量即生成的二氧化碳质量,生成的二氧化碳质量为4.4g。
(2)设参加反应的碳酸钙的质量为x
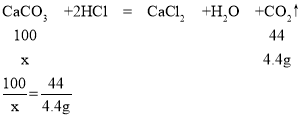
x=10g
该石灰石中碳酸钙的质量分数为![]() ×100%≈66.7%。
×100%≈66.7%。
答:(1)生成的二氧化碳质量为4.4。
(2)该石灰石中碳酸钙的质量分数为66.7%。

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目