题目内容
【题目】盐酸与氢氧化钠溶液反应时溶液 pH 的变化如图所示。
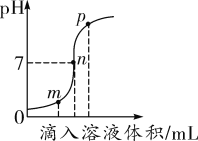
(1)根据图示判断,该实验是将_____(填“氢氧化钠溶液”或“盐酸”)滴加到另一种溶液中。
(2)取m 点时的溶液在蒸发皿中蒸干,得到物质为_____。
(3)在测定p 点溶液的pH 时,若用用水润试过的 pH 试纸测量,会使测量结果_____(填“偏大”、“偏小”或“不受影响”)
【答案】氢氧化钠溶液 氯化钠 偏小
【解析】
盐酸和氢氧化钠生成氯化钠和水。
(1)由图可知,开始pH小于7,随着溶液的滴加,pH逐渐增大,最终溶液的pH大于7,故该实验是将氢氧化钠溶液滴加到另一种溶液中。
(2)m点时,溶液的pH小于7,盐酸过量,盐酸和氢氧化钠生成氯化钠和水,m点溶液中含有的溶质氯化钠和氯化氢气体,故取m点时的溶液在蒸发皿中蒸干,得到物质为氯化钠。
(3)p点溶液pH大于7,溶液呈碱性,用水润湿pH试纸,相当对溶液稀释,溶液的碱性减弱,pH减小,故在测定p点溶液的pH时,用水润湿过的pH试纸测量,会使测量结果偏小。

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
【题目】“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56g)
甲 | 乙 | 丙 | |
烧杯+稀盐酸质量 | 139g | 129g | 129g |
加入黄铜样品质量 | 20g | 24g | 20g |
充分反应后,烧杯+剩余物质质量 | 158.8g | 152.8g | 148.8g |
发生的反应化学方程式:Zn+2HCl=ZnCl2+H2↑,请回答下列问题:
(1)同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是____________。
(2)所用的稀盐酸的溶质质量分数。____________