题目内容
【题目】某化学课堂围绕“酸碱中和反应”, 将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格。
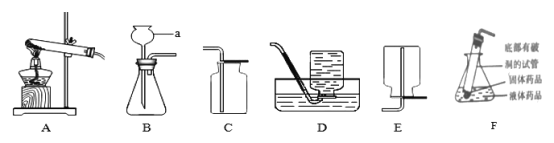
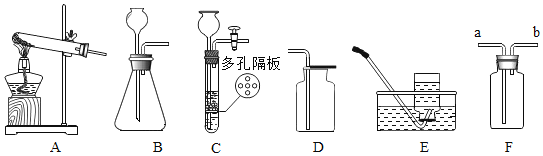
(演示实验)将一定量的氢氧化钙溶液加入到盛稀盐酸的小烧杯中,该反应的化学方程式是_______________________________。
(查阅资料)CaCl2溶液显中性。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(猜想与假设)针对疑问,甲组同学的猜想如下:
猜想Ⅰ:只有___________猜想Ⅱ:有CaCl2和HCl
猜想Ⅲ:有CaCl2和Ca(OH)2 猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为有一种猜想Ⅳ不合理,其理由是______________________。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实 验 步 骤 | 实验现象 | 结论 | |
方案1 | 取少量烧杯内溶液于试管中,滴入几滴紫色石蕊溶液,振荡。 | ___________ | 溶液中 含有 Ca(OH)2 |
方案2 | 取少量烧杯内溶液于另一试管中,通入CO2气体 | ___________ | |
方案3 | 再取少量烧杯内溶液于另一试管中,滴加碳酸钠溶液,振荡。 | 产生白色沉淀 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________________________。
(2)分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还要考虑_______________。
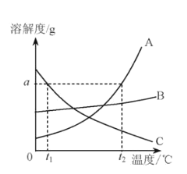
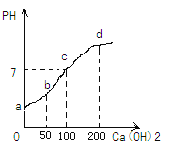
(拓展延伸)15℃时,向一定量的10%盐酸中滴加质量分数为0.148%的氢氧化钙溶液,溶液的pH与所加氢氧化钙溶液的质量(克)如图所示,则b点对应的溶液中溶质是_________;向d点对应的溶液中滴加无色的酚酞溶液,溶液呈_____色;根据c点时数据可知,稀盐酸的质量为______g.
【答案】![]() CaCl2 HCl和Ca(OH)2不能共存 石蕊溶液变蓝 溶液变浑浊 CaCl2与Na2CO3反应也会成生成白色沉淀,不能证明一定有Ca(OH)2存在 反应物是否过量 HCl和CaCl2 红 1.46
CaCl2 HCl和Ca(OH)2不能共存 石蕊溶液变蓝 溶液变浑浊 CaCl2与Na2CO3反应也会成生成白色沉淀,不能证明一定有Ca(OH)2存在 反应物是否过量 HCl和CaCl2 红 1.46
【解析】
[演示实验] 将一定量的氢氧化钙溶液加入到盛稀盐酸的小烧杯中,反应为氯化氢和氢氧化钙反应生成氯化钙和水,该反应的化学方程式是![]() ;刚好完全反应时,反应后溶液中的溶质只有氯化钙,猜想Ⅰ:只有CaCl2;猜想Ⅳ不合理,其理由是氢氧化钙和氯化氢不共存;
;刚好完全反应时,反应后溶液中的溶质只有氯化钙,猜想Ⅰ:只有CaCl2;猜想Ⅳ不合理,其理由是氢氧化钙和氯化氢不共存;
[实验探究] 方案1:氢氧化钙溶液呈碱性,能使紫色石蕊试液变蓝;方案2:氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,取少量烧杯内溶液于另一试管中,通入CO2气体,可观察到溶液变浑浊;
[评价反思] (1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,因为氯化钙和氢氧化钙都能与碳酸钠反应生成碳酸钙沉淀,向溶液中滴加碳酸钠生成沉淀,不能证明一定有Ca(OH)2存在;
(2)分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还要考虑反应物是否过量(反应物是否有剩余);
[拓展延伸]由图可知,C点时氢氧化钙和盐酸刚好完全反应,此时氢氧化钙溶液的质量为100g,而b点氢氧化钙溶液的质量50g,盐酸有剩余,此时溶液中的溶质有生成的氯化钙和剩余的氯化氢;因d点氢氧化钙溶液有剩余,溶液呈显碱性,向d点对应的溶液中滴加无色的酚酞溶液,溶液呈红色;设稀盐酸中溶质的质量为x,
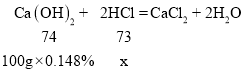
![]()
x=0.146g
则稀盐酸溶液的质量为:0.146g÷10%=1.46g

 名校课堂系列答案
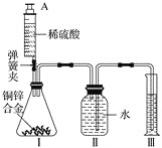
名校课堂系列答案【题目】小明对铁的锈蚀进行如下探究,室温时,将包有样品的滤纸包用大头针固定在橡胶塞上,迅速塞紧,装置如图,观察到量筒内水沿导管慢慢进入广口瓶(净容积为146mL)。当温度恢复至室温,且量筒内水面高度不变时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如表。
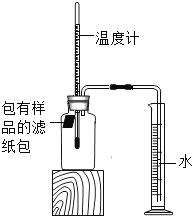
序号 | 样品 | 量筒起始 读数/mL | 量筒最终 读数/mL | 所需时间 /min |
1 | 1g铁粉、0.2g碳和10滴水 | 100 | 70 | 约120 |
2 | lg铁粉、0.2g碳、10滴水和少量NaCl | 100 | 70 | 约70 |
3 | …… | 100 | 70 | 约480 |
(1)实验①和②说明NaCl可以_____铁锈蚀的速率。
(2)实验开始后,广口瓶内温度有所上升,说明铁的锈蚀过程是_____(填“放热”或“吸热”)过程。
(3)实验结束后取出滤纸包,观察到有红棕色物质生成,该物质的化学式是_____。
(4)已知含碳能够加快铁的生锈速度,小明想通过实验①和③是探究碳对铁锈蚀速率的影响,请在表格空白处填写实验③的样品组成_____。
(5)该装置还可用于测量空气中氧气的含量,根据上述数据计算氧气的体积含量是_____(小数点后保留1位)。