题目内容
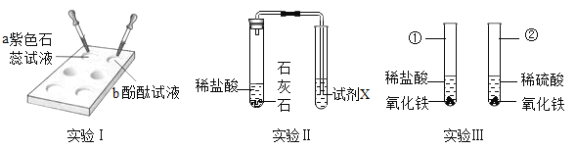
【题目】化学是一门以试验为基础的科学,某校化学兴趣小组用如图所示的装置完成实验,请根据要求回答问题:
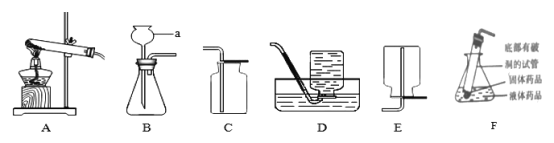
(1)写出仪器a的名称_____,小刚在实验室想用同一个装置制取氧气和二氧化碳,应选择的发生装置和收集装置是_____,请写出用此装置制取氧气的化学方程式_____,实验中发现不能得到平稳的氧气流,小红同学提出可以从两个方面加以改进:
一是改进发生装置,方法为_____;
二是将过氧化氢溶液加水稀释。如果把50g溶质质量分数为15%的过氧化氢溶液稀释成溶质质量分数为10%的溶液,需加水的质量_____g。
(2)实验室制取二氧化碳的化学方程式为_____,F是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点_____。
【答案】长颈漏斗 BC 2H2O2![]() 2H2O+O2↑ 将装置B中的长颈漏斗换为分液漏斗 25 CaCO3+2HCl=CaCl2+H2O+CO2↑ 能随时控制反应的发生与停止
2H2O+O2↑ 将装置B中的长颈漏斗换为分液漏斗 25 CaCO3+2HCl=CaCl2+H2O+CO2↑ 能随时控制反应的发生与停止
【解析】
(1)由图可知,仪器a的名称是长颈漏斗,故填长颈漏斗;
制取氧气和二氧化碳均能采用固体与液体在常温条件下反应,应选择固液常温发生装置,即B,氧气与二氧化碳的密度均大于空气的密度,都可采用向上排空气法收集,即C,故填BC;
选用发生装置B制取氧气的反应是过氧化氢在二氧化锰作催化剂的条件下反应生成水和氧气,故反应的化学方程式写为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
将固液常温发生装置中的长颈漏斗换为分液漏斗,通过调节玻璃开关可以控制滴加过氧化氢溶液的速率,进而控制反应的速率,故填将装置B中的长颈漏斗换为分液漏斗;
设加入水的质量为x
50g×15%=(50g+x)×10%
x=25g,故填25。
(2)实验室制取二氧化碳的反应是石灰石中的碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
反应中,将试管从液体中取出,反应停止,再将试管伸进液体中,反应继续进行,即能随时控制反应的发生与停止,故填能随时控制反应的发生与停止。

【题目】某化学课堂围绕“酸碱中和反应”, 将学生分成若干小组,在老师引导下开展探究活动。以下是教学片段,请你参与学习并帮助填写空格。
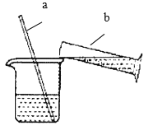
(演示实验)将一定量的氢氧化钙溶液加入到盛稀盐酸的小烧杯中,该反应的化学方程式是_______________________________。
(查阅资料)CaCl2溶液显中性。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(猜想与假设)针对疑问,甲组同学的猜想如下:
猜想Ⅰ:只有___________猜想Ⅱ:有CaCl2和HCl
猜想Ⅲ:有CaCl2和Ca(OH)2 猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为有一种猜想Ⅳ不合理,其理由是______________________。
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
实 验 步 骤 | 实验现象 | 结论 | |
方案1 | 取少量烧杯内溶液于试管中,滴入几滴紫色石蕊溶液,振荡。 | ___________ | 溶液中 含有 Ca(OH)2 |
方案2 | 取少量烧杯内溶液于另一试管中,通入CO2气体 | ___________ | |
方案3 | 再取少量烧杯内溶液于另一试管中,滴加碳酸钠溶液,振荡。 | 产生白色沉淀 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)
(1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因____________________________。
(2)分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还要考虑_______________。
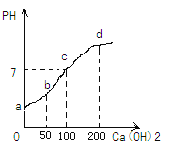
(拓展延伸)15℃时,向一定量的10%盐酸中滴加质量分数为0.148%的氢氧化钙溶液,溶液的pH与所加氢氧化钙溶液的质量(克)如图所示,则b点对应的溶液中溶质是_________;向d点对应的溶液中滴加无色的酚酞溶液,溶液呈_____色;根据c点时数据可知,稀盐酸的质量为______g.
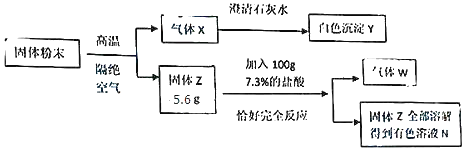
【题目】为测定CuCl2和FeCl2组成的混合溶液中FeCl2的质量分数,进行如下实验:
①取200g混合溶液加入足量的AgNO3溶液,经过滤、洗涤、干燥、称量,得到143.5gAgCl固体;②另取原混合溶液各200g与含有杂质的废铁屑反应(杂质不溶于水,也不参与反应),共做了五组实验,其实验数据如下表。
实验组别 | 一 | 二 | 三 | 四 | 五 |
混合溶液质量/g | 200 | 200 | 200 | 200 | 200 |
铁屑质量/g | 6 | 9 | 12 | 15 | 18 |
析出铜的质量/g | 6.4 | 9.6 | m | 16 | 16 |
请分析计算:
(1)表中第三组实验的m值为_______。
(2)第_____组实验恰好完全反应。
(3)铁屑中铁的质量分数为多少___________?(计算结果精确到0.1%)
(4)原混合溶液中FeCl2的质量分数为多少______________?(计算结果精确到0.1%)
【题目】阅读下面科普短文。
目前我国空气质量常规监测的项目为二氧化硫(SO2)、二氧化氮(NO2)、可吸入颗粒(PM10)、细颗粒物(PM2.5)、一氧化碳(CO)和臭氧(O3)。某研究小组依据2005-2016年的监测数据,研究中国部分污染物的时间分布特征,结果如下。
表1 部分污染物随季节变化的统计数据
首要 污染物 | 出现天数占总污染天数的比例(%) | ||||
春季 | 夏季 | 秋季 | 冬季 | ||
PM10 | 68.64 | 55.13 | 63.63 | 59.75 | |
SO2 | 4.3 | 2.11 | 4.13 | 13.32 | |
NO2 | 1.08 | 0.46 | 1.15 | 1.1 | |
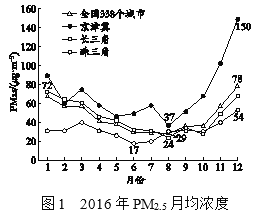
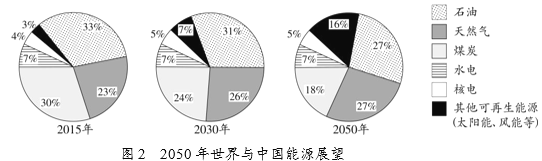
2016年1月1日全国实施新的《环境空气质量标准》。新标准提高了对某些污物的控制标准和限值要求,衡量空气质量的“尺子”更严了。北京市为提升空气质量,依据研究结果、能源发展趋势(图2) 、城市特点等制定综合整治方案,如调整燃煤锅炉的能源、平房的“煤改电”、减少汽车尾气排放等。综合整治使北京市这样的北方超大型冬季供暖城市的污染物浓度得到了有效控制。
依据文章内容回答下列问题。
(1)空气质量监测项目中,属于氧化物的是______(至少答两种)。
(2)依据图1可知,全国PM2.5月均浓度变化特征是______。
(3)对北京市采取的整治措施进行分析。
①结合表1分析,冬季供暖“煤改电”可使______污染物的排放降幅最明显。
②由图2可知,未来能源结构中所占比例日益增多的能源有天然气和______。
③三元催化器可净化汽车尾气,其主要反应的微观示意图如下,请补全图中微粒______。

【题目】牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如![]() 、
、![]() 、
、![]() 或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分.
或这些物质的混合物.我校兴趣小组想研究牙膏摩擦剂的成分.
(提出问题1)某品牌牙膏中是否含有![]() ?
?
(查阅资料)二氧化硅不与稀盐酸反应
(实验方案)
①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,证明摩擦剂中含有______离子;
②取实验①中的溶液,加入草酸铵(![]() )溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式______.
)溶液,生成白色沉淀--草酸钙,请写出该反应的化学方程式______.
(提出问题2)该牙膏中![]() 的含量是多少?
的含量是多少?
(实验装置)
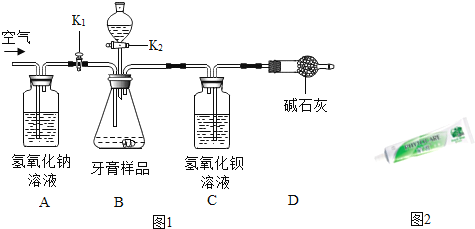
(实验步骤)
(1)按如图连接好装置后,发现一处明显的错误,改正为______;
(2)重新连接好装置,并检查装置的气密性;
(3)在B装置中加入牙膏样品8.00g;
(4)关闭K1,打开K2(填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至B中不再产生气泡,停止滴加盐酸;
(5)关闭K2,打开K1,缓缓通入空气,至C中不再产生沉淀;
(6)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(7)重复实验.(已知此品牌牙膏中的摩擦剂为碳酸钙,且其他成分不和盐酸反应,装置内试剂均足量.)
(实验数据)重复实验,3次数据记录如表:
实验次数 | 实验1 | 实验2 | 实验3 |
C装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(实验分析及数据处理)
(1)上述数据能否由托盘天平测得?______.
(2)若没有A装置,则测定结果将______.(填“偏大”、“偏小”或“不变”)
(3)D装置的作用是______.
(4)据上表数据,计算该牙膏样品中![]() 的含量是多少?写出计算过程______.
的含量是多少?写出计算过程______.
(实验反思)
(1)重复实验,取平均值的意义在于减小偶然误差(合理即可).
(2)下列各项措施中,能提高测定准确度的是______(填序号).
a 在装置A、B之间增加盛有浓硫酸的洗气瓶
b 在装置B、C之间增加盛有饱和碳酸氢钠的洗气瓶
c 缓缓滴加稀盐酸.