题目内容
【题目】通过观察和实验的方法可获知物质的性质,从物质的状态、颜色、温度变化、有无沉淀或气体生成等方面可寻找物质发生变化的证据,分析各种证据能加深对物质变化和变化规律的认识。请回答:
(1)将锌粒放入稀硫酸中,锌粒表面产生气泡,产生该气泡的化学方程式为________________________;该反应的基本类型属于________________________反应。
(2)经引燃的铁丝在氧气中燃烧,支持铁和氧气发生化学反应的最主要证据是________________________;
(3)我国西汉时期,在《淮南万毕术》中记载“曾青得铁则化为铜”,意思是可溶性的铜的化合物与铁发生反应得到单质铜。该反应证明了铁的金属活动性比铜________________________。 某大型工厂利用此原理处理含硫酸铜的废液回收金属铜时,向100kg 的废液中加入足量的铁粉,得到金属铜6.4kg,那么废液中硫酸铜的质量分数是________________________。
(4)铁是应用广泛的金属,但每年因锈蚀而报废的数量也相当惊人。请写出你所知道的一种防止铁制品生锈的方法:________________________。(写出 一种即可)
【答案】![]() 置换反应 生成黑色固体四氧化三铁 强 16% 在铁制品表面刷漆
置换反应 生成黑色固体四氧化三铁 强 16% 在铁制品表面刷漆
【解析】
(1)将锌粒放入稀硫酸中,锌粒表面产生气泡,锌与稀硫酸反应生成硫酸锌和氢气,其化学反应方程式为:![]() ;
;
该反应符合一种单质与一种化合物生成另一种单质和另一种化合物的反应,属于置换反应;
(2)铁丝在氧气中剧烈燃烧、火星四射,生成黑色固体,化学反应的本质是有新物质生成,故支持铁和氧气发生化学反应的最主要证据是生成黑色固体四氧化三铁;
(3)可溶性的铜的化合物与铁发生反应得到单质铜,说明铁能将铜从铜的化合物的溶液里置换出来,故该反应证明了铁的金属活动性比铜强;
设废液中硫酸铜的质量分数是x
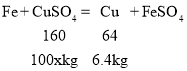
![]() x=16%
x=16%
故废液中硫酸铜的质量分数是16%;
(4)铁生锈是因铁与氧气、水直接接触,故防止铁制品生锈,可采取在铁制品表面刷漆,或将铁制品置于干燥的环境中等方法。

 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案