题目内容
 将质量相等的a、b、c三块金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如图所示(产物中a、b、c三种元素的化合价相同).分析图,可以获得:
将质量相等的a、b、c三块金属,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如图所示(产物中a、b、c三种元素的化合价相同).分析图,可以获得:(1)活泼性
(2)相对原子质量
考点:金属的化学性质
专题:金属与金属材料
分析:根据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
根据一定质量的金属完全反应产生氢气的质量=
×反应的金属的质量,结合三种金属的化合价及完全反应放出氢气的质量大小,判断三种金属的相对原子质量的大小.
根据一定质量的金属完全反应产生氢气的质量=
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:(1)根据坐标可以发现,单位时间内a产生的氢气比c多,c比b多,故a的反应速度快,其次是c、b,故三种金属的活动性强弱顺序为:a>c>b;
(2)三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是a>b>c;因此可判断相对原子质量是c>b>a;
故答案为:(1)a>c>b;(2)c>b>a.
(2)三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是a>b>c;因此可判断相对原子质量是c>b>a;
故答案为:(1)a>c>b;(2)c>b>a.
点评:本题考查了金属活动性顺序的应用,对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
下列自然灾害发生时,其主要变化为化学变化的是( )
| A、台风 | B、雪灾 |
| C、山体滑坡 | D、森林火灾 |
 表示氯原子,
表示氯原子, 表示氧原子,
表示氧原子, 表示氢原子)
表示氢原子)
 (1)用“
(1)用“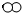 ”和“
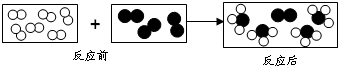
”和“ ”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:写出上述过程发生的化学反应的方程式:
”分别代表两种不同的单质分子A2和B2,它们在一定条件下能发生化学反应,其反应的微观示意图如图:写出上述过程发生的化学反应的方程式: