题目内容
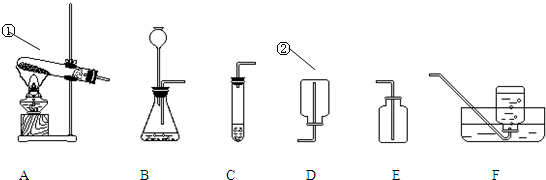
根据下列装置图回答问题.
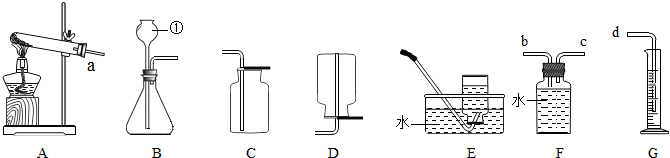
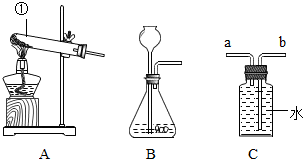
(1)标号仪器①的名称是
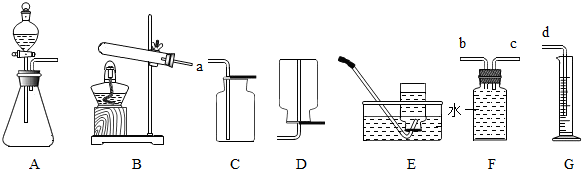
(2)实验室制取二氧化碳,应选择的发生装置和收集装置为
(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积(装置选用A、F、G).
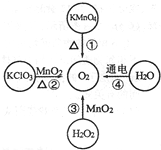
①写出该反应的化学方程式
②根据高锰酸钾的质量算出的氧气体积为理论值.如果实际测得氧气的体积大于理论值(水的体积测量准确),你认为原因是
③若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后固体混合物中的质量分数将

(1)标号仪器①的名称是
长颈漏斗
长颈漏斗
.(2)实验室制取二氧化碳,应选择的发生装置和收集装置为
B、C
B、C
(填字母序号).(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积(装置选用A、F、G).
①写出该反应的化学方程式
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.
| ||
②根据高锰酸钾的质量算出的氧气体积为理论值.如果实际测得氧气的体积大于理论值(水的体积测量准确),你认为原因是
未冷却到室温就读数
未冷却到室温就读数
.③若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后固体混合物中的质量分数将
变大
变大
(填“变大”、“变小”或“不变”).分析:(1)了解常用的仪器名称、用法、选取和连接方法;
(2)实验室制取二氧化碳,应选择的发生装置和收集装置:考虑反应原理和气体的密度和水溶性;
(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积:
①正确书写高锰酸钾制取氧气的化学方程式;
②了解正确读数的时机,待冷却到室温再读数;
③根据化学方程式分析二氧化锰在反应前后固体混合物中的质量分数的变化.
(2)实验室制取二氧化碳,应选择的发生装置和收集装置:考虑反应原理和气体的密度和水溶性;
(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积:
①正确书写高锰酸钾制取氧气的化学方程式;
②了解正确读数的时机,待冷却到室温再读数;
③根据化学方程式分析二氧化锰在反应前后固体混合物中的质量分数的变化.
解答:解:(1)熟记常用仪器:长颈漏斗;
(2)制取二氧化碳的药品是石灰石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是B;因为二氧化碳能溶于水,密度比空气大,故收集装置C;
(3)①高锰酸钾制取氧气的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑;
②如果实际测得氧气的体积大于理论值(水的体积测量准确),原因是未冷却到室温就读数;
③根据化学方程式2KClO3
2KCl+3O2↑可知,由于氧气逸出,因此二氧化锰在反应前后固体混合物中的质量分数应变大.
故答为:(1)长颈漏斗;
(2)B、C;
(3)①2KMnO4
K2MnO4+MnO2+O2↑;
②未冷却到室温就读数;
③变大.
(2)制取二氧化碳的药品是石灰石和稀盐酸,属于固体和液体在常温下的反应,因此应选用的发生装置是B;因为二氧化碳能溶于水,密度比空气大,故收集装置C;
(3)①高锰酸钾制取氧气的化学方程式为2KMnO4
| ||
②如果实际测得氧气的体积大于理论值(水的体积测量准确),原因是未冷却到室温就读数;
③根据化学方程式2KClO3
| ||
| △ |
故答为:(1)长颈漏斗;
(2)B、C;
(3)①2KMnO4
| ||
②未冷却到室温就读数;
③变大.
点评:本题主要考查了实验室根据反应原理和气体的密度和水溶性制取氧气、二氧化碳的装置的选取;了解常用气体的收集方法;根据题目中的信息正确有关书写化学方程式.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目