题目内容
【题目】如下图是自来水消毒过程中发生反应的微观示意图,产物之一是次氯酸(HClO),具有杀菌消毒作用.
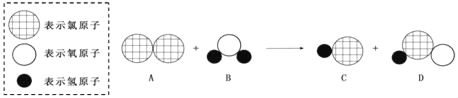
(1)该反应的化学方程式为_____.
(2)该微观示意图中属于化合物的共有_____ 种.
(3)上述反应D物质中,氯元素的化合价是_____.
(4)上述反应D物质中的酸根是_____.(写离子符号)
(5)为证明该反应已发生,可通过检验部分产物来进行判断,具体方法是_____.
【答案】 Cl2+H2O=HCl+HClO 3 +1 ClO﹣ 取样品少许于试管中,滴加适量的硝酸银溶液,若有白色沉淀生成,说明已经发生反应
【解析】(1)由微观示意图可知,A物质是Cl2,B是H2O,C是HCl,D是HClO,根据质量守恒定律,反应方程式为:Cl2+H2O=HCl+HClO;
(2)化合物是指由多种元素组成的纯净物,图中,B、C、D是由多种元素组成,是化合物,故有三种化合物;
(3)D物质是HClO,其中氢元素的化合价是+1价,氧元素的化合价是-2价,设氯元素的化合价为x,根据化合价的代数和为0,+1+x+(-2)=0,x=+1;
(4)D物质是次氯酸,在水溶液中电离出氢离子和次氯酸根离子,故酸根离子是ClO﹣ ;
(5)氯气和水反应后有盐酸和次氯酸生成,盐酸可以与硝酸银反应有白色沉淀生成,故具体步骤是:取样品少许于试管中,滴加适量的硝酸银溶液,若有白色沉淀生成,说明已经发生反应。

 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案【题目】下表列出了固体物质A在不同温度时的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是______________(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____________(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线应是右图中的___________(填“甲”或“乙”);

(3)80℃时,配制一定量A物质的溶液,将其降温到60℃,是否有固体析出?____________(填“有”、 “没有”或“不确定”)。