题目内容
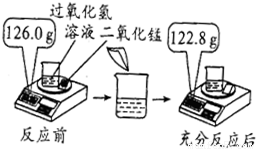
为测定实验室中某过氧化氢溶液中过氧化氢的质量,小明取25.0g过氧化氢溶液放入烧杯中,然后进行如图所示的实验.请计算:
(1)反应后产生氧气的质量为多少克?
(2)此过氧化氢溶液中过氧化氢的质量是多少克?
【答案】分析:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.因此完全反应后,物质减少的质量就是生成的气体质量;
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量.
解答:解:(1)根据质量守恒定律,反应生成氧气的质量=126.0g-122.8g=3.2g;
(2)解:设25.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 2H2O+O2↑
2H2O+O2↑
68 32
x.3.2g

解之得:x=6.8g
答:(1 )生成氧气的质量是3.2g;(2)溶液中过氧化氢的质量为6.8g;
点评:本题主要考查学生根据质量守恒定律,运用化学方程式和质量分数公式进行计算的能力.
(2)根据过氧化氢分解的化学方程式和(1)中计算出的氧气的质量,就可计算出参与反应的过氧化氢的质量.
解答:解:(1)根据质量守恒定律,反应生成氧气的质量=126.0g-122.8g=3.2g;
(2)解:设25.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2
 2H2O+O2↑
2H2O+O2↑68 32
x.3.2g

解之得:x=6.8g
答:(1 )生成氧气的质量是3.2g;(2)溶液中过氧化氢的质量为6.8g;
点评:本题主要考查学生根据质量守恒定律,运用化学方程式和质量分数公式进行计算的能力.

练习册系列答案
相关题目
(9分)实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神。
(一)实验室制取气体是初中一类重要的实验,结合下列仪器或装置图回答有关问题: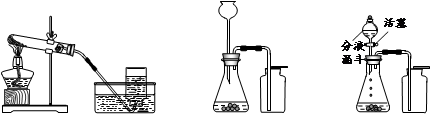
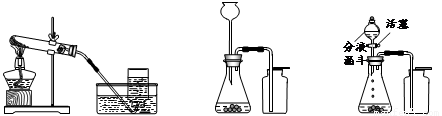
装置I 装置Ⅱ 装置Ⅲ
(1)装置I是用高锰酸钾制氧气,反应的化学方程式为_________________________,表明氧气已经收满的实验现象是 。
(2)某同学用装置Ⅱ制取并收集二氧化碳,用燃着的木条放在集气瓶口验满,始终未发现火焰熄灭,原因是______________________________________________。
(3)用装置Ⅲ进行二氧化锰和双氧水制取氧气的实验时,若反应速率过快,可以采取的处理方法是 。
(4)我们已经学过实验室制取O2、CO2、H2三种气体的反应原理及制取、收集方法。请你归纳出制取这三种气体时反应的共同点_______(填选项序号)。
| A.需要加热 | B.需使用催化剂 |
| C.没有气体参加反应 | D.生成的气体只有一种 |
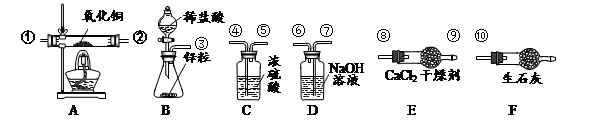
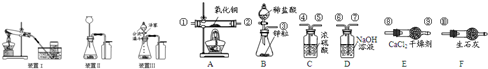
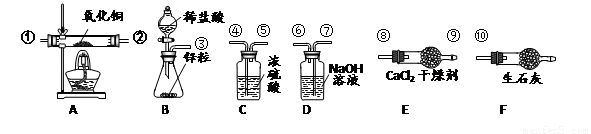
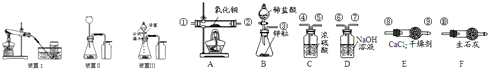
(5)为准确测定水的组成并防止杂质、空气等干扰,导管口的正确连接顺序为:
③→___→____→____→____→①→②→⑧→⑨→⑩。
(6)若测得A装置中样品在实验后减少了6.4克,E装置质量增加了7.2克,F装置增加了0.1克,据此可求出水中H、O元素质量比为(只写计算式)____________。
(7)实验结束后,若A处仍有黑色固体,这对实验结果的影响是________________(填“氧的质量偏大”、“氢的质量偏大”、“无影响”)。