题目内容
【题目】工业上用纯碱和石灰石为原料制备烧碱的简要工艺流程如下图所示
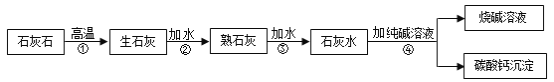
(1)石灰石、生石灰、熟石灰均能与下列___________(填字母)发生化学反应。
A水 B.盐酸 C二氧化碳 D草木灰
(2)写出上述工艺流程中第四步的化学反应方程式______________。
(3)某研究性学习小组的同学想检验上述工艺中的烧碱溶液里是否含有纯碱,甲同学选择了一种酸溶液,乙同学选择了一种碱溶液,丙同学选择了一种盐溶液,他们都能达到检验目的。请在下表中写出甲乙丙所用物质的化学式
甲 | 乙 | 丙 |
______ | _______ | _________ |
(4)步骤④中检验碳酸钙沉淀已洗涤干净的方法是_____________。
【答案】B ![]() HCl或H2SO4 Ca(OH)2或Ba(OH)2 CaCl2或BaCl2 取最后一次的洗涤液样品于试管中,滴加酚酞,如果酚酞变红则没有洗干净,如果不变红,则洗涤干净
HCl或H2SO4 Ca(OH)2或Ba(OH)2 CaCl2或BaCl2 取最后一次的洗涤液样品于试管中,滴加酚酞,如果酚酞变红则没有洗干净,如果不变红,则洗涤干净
【解析】
(1)石灰石的主要成分CaCO3是碳酸盐,生石灰是金属氧化物、熟石灰是碱,它们均能与稀盐酸发生化学反应,故选B。
(2)上述工艺流程中第四步发生的反应是氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,其化学反应方程式为:![]() 。
。
(3)碳酸钠中含有碳酸根离子,它能跟足量的稀盐酸、稀硫酸反应生成二氧化碳;能跟氢氧化钙、氢氧化钡溶液反应生成碳酸钙、碳酸钡沉淀;能跟氯化钙、氯化钡溶液反应生成碳酸钙、碳酸钡沉淀,因此甲同学选择的一种酸溶液是:HCl或H2SO4,乙同学选择的一种碱溶液是:Ca(OH)2或Ba(OH)2,丙同学选择的一种盐溶液是:CaCl2或BaCl2(合理即可)。
(4)步骤④中,碳酸钙沉淀是否洗涤干净,可根据洗涤液中是否含有氢氧化钠来判断。因此检验碳酸钙沉淀已洗涤干净的方法是:取最后一次的洗涤液样品于试管中,滴加酚酞,如果酚酞变红则没有洗干净,如果不变红,则洗涤干净(合理即可)。