题目内容
【题目】如图所示为实验室中常见的气体制备和收集装置. 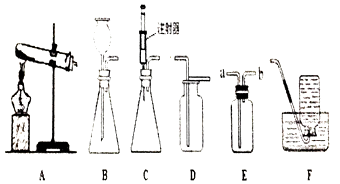
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置(填字母需和),反应的化学方程式为 , 若用装置D收集氧气,验满的方法是 .
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是 .
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从(填“a”或“b”)端通入,欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从(填“a”或“b“)端通入.
【答案】
(1)A;2KMnO4![]() K2MnO4+MnO2+O2↑;将带火星的木条置于集气瓶口,若木条复燃,则氧气已满
K2MnO4+MnO2+O2↑;将带火星的木条置于集气瓶口,若木条复燃,则氧气已满
(2)控制氧气产生的快慢和量的多少
(3)a;b
【解析】解:(1)实验室用加热分解高锰酸钾的方法制取氧气的化学反应式是:2KMnO4 ![]() K2MnO4+MnO2+O2↑;此反应是固体的加热反应,A装置适用于固体的加热反应,故可选A作为发生装置;因氧气有助燃的性质,验满时可将带火星的木条置于集气瓶口,若木条复燃,则氧气已满.
K2MnO4+MnO2+O2↑;此反应是固体的加热反应,A装置适用于固体的加热反应,故可选A作为发生装置;因氧气有助燃的性质,验满时可将带火星的木条置于集气瓶口,若木条复燃,则氧气已满.
所以答案是:A;2KMnO4 ![]() K2MnO4+MnO2+O2↑;A;将带火星的木条置于集气瓶口,若木条复燃,则氧气已满;(2)C装置中用的是注射器,它的优点是:控制氧气产生的快慢和量的多少;故填:控制氧气产生的快慢和量的多少;(3)欲使用装置E用排空气法收集二氧化碳,因为二氧化碳的密度比空气的密度大,因此应该从a进入.欲使用装置E用排水法收集氧气,先将瓶中装满水,因为气体的密度总比水的密度小,因此再将气体从b进入即可,所以答案是:a;b.
K2MnO4+MnO2+O2↑;A;将带火星的木条置于集气瓶口,若木条复燃,则氧气已满;(2)C装置中用的是注射器,它的优点是:控制氧气产生的快慢和量的多少;故填:控制氧气产生的快慢和量的多少;(3)欲使用装置E用排空气法收集二氧化碳,因为二氧化碳的密度比空气的密度大,因此应该从a进入.欲使用装置E用排水法收集氧气,先将瓶中装满水,因为气体的密度总比水的密度小,因此再将气体从b进入即可,所以答案是:a;b.
【考点精析】认真审题,首先需要了解氧气的制取装置(发生装置:固固加热型、固液不加热型),还要掌握氧气的收集方法(收集装置:根据物质的密度、溶解性;排水法收集时,待气泡均匀连续冒出时再收集(刚开始排出的是试管中的空气;)用排空气法收集气体时,导管伸到集气瓶底部)的相关知识才是答题的关键.

 名校课堂系列答案
名校课堂系列答案【题目】某实验小组的同学用氢氧化钙溶液和稀盐酸做中和反应实验时,向烧杯中的氢氧化钙溶液加入一定量稀盐酸后,发现忘记了滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
(1)Ⅰ.写出该中和反应的化学方程式:。
(2)Ⅱ.探究烧杯内溶液中溶质的成分。
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】甲、乙、丙三位同学分别作出了猜想,请你补充丁同学的猜想。
同学甲:可能是CaCl2和Ca(OH)2; 同学乙:可能只有CaCl2;
同学丙:可能是CaCl2、HCl和Ca(OH)2 同学丁:可能是。
你认为该小组同学的猜想中不需做实验就可以否定的是。
(3)【查阅资料】氯化钙溶液呈中性。
【进行实验】
实验步骤 | 实验操作 | 实验现象 | 实验结论 |
实验1 | 取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 | 同学甲猜想不正确 | |
实验2 | 另取少量烧杯内溶液于试管中,逐滴加入碳酸钠溶液至过量 | 先有 , 后有。 | 同学丁猜想正确 |
(4)【反思与拓展】
①在分析化学反应后所得物质成分时,除考虑生成物外还需考虑。
②根据所学化学知识,验证烧杯内溶液中的溶质是否含有Ca(OH)2 , 除以上方案外,下列哪些物质单独使用也能完成该实验?(填序号)
a.pH试纸 b.铜 c.二氧化碳 d.氧化铜
(5)Ⅲ.取10g烧杯中的溶液,向其中逐滴滴入溶质质量分数为5.3%的碳酸钠溶液,同时充分搅拌。测得溶液pH与加入的碳酸钠溶液的质量关系如图所示。
①由图可知,当碳酸钠溶液质量加到 g时,溶液中盐酸恰好反应完;
②原烧杯溶液中氯化钙的质量分数。(写出计算过程)