题目内容
(2013?海安县模拟)金属材料、无机非金属材料、有机合成材料是人类使用的三大类基础材料,它们在生产、生活中有着广泛的应用.
(1)金属材料:
①在下列应用中使用金属材料的有

②人类每年都从自然界中提取数以亿吨的金属.工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁的化学方程式为
(2)无机非金属材料:
硅(Si)是太阳能电池和电脑芯片不可缺少的无机非金属材料.工业上利用石英沙(主要成分为二氧化硅)生产高纯硅的流程示意图如下: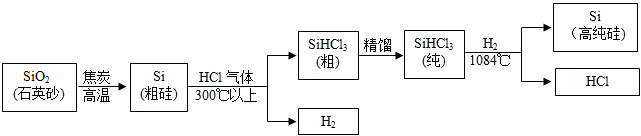
①整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,可能引起的后果是
②为了达到绿色化学和资源综合利用的目的,上述生产流程中可以循环使用的物质有
③生产高纯硅前需要对普通石英砂(含有少量的CaCO3和Fe2O3)进行提纯,其中酸洗(用盐酸)和水洗是两个重要的步骤.请写出酸洗步骤中的一个化学反应方程式:
(3)有机合成材料:
2011年9月27日第十一届中国塑料交易会在台州市国际会展中心落下帷幕.其中超高分子量聚乙烯制成的防弹背心、防刺手套、聚丙烯制成的奥迪A6保险杠等都是本次塑料交易会重要产品之一.你认为下列制品的主要成分不属于有机合成材料的是
A.聚乙烯制成的防弹背心、防刺手套 B.化学实验室常用的胶皮导管 C.纯棉内衣 D.锦纶制成的尼龙袜子 E. 聚丙烯制成的奥迪A6保险杠 F.真丝围巾.
(1)金属材料:
①在下列应用中使用金属材料的有
A、C
A、C
(填字母).
②人类每年都从自然界中提取数以亿吨的金属.工业上用一氧化碳和赤铁矿(主要成分是氧化铁)冶炼铁的化学方程式为
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
;我国还是世界上最早采用湿法冶金炼铜的国家,写出铁与硫酸铜溶液反应制取铜的化学方程式
| ||
Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.铝的化学性质比铁和铜都要活泼,但其抗锈蚀性比铁和铜都要强,原因是铝与空气中的氧气反应生成致密的氧化物薄膜,使其不易生锈
铝与空气中的氧气反应生成致密的氧化物薄膜,使其不易生锈
.(2)无机非金属材料:
硅(Si)是太阳能电池和电脑芯片不可缺少的无机非金属材料.工业上利用石英沙(主要成分为二氧化硅)生产高纯硅的流程示意图如下:

①整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,可能引起的后果是
氢气不纯,可能爆炸
氢气不纯,可能爆炸
(填一种可能).②为了达到绿色化学和资源综合利用的目的,上述生产流程中可以循环使用的物质有
稀盐酸
稀盐酸
.③生产高纯硅前需要对普通石英砂(含有少量的CaCO3和Fe2O3)进行提纯,其中酸洗(用盐酸)和水洗是两个重要的步骤.请写出酸洗步骤中的一个化学反应方程式:
CaCO3+2HCl═CaCl2+CO2↑+H2O
CaCO3+2HCl═CaCl2+CO2↑+H2O
;判断水洗是否洗净的方法是取少量最后的洗涤液于试管中,向其中滴加少量AgNO3溶液,若无白色沉淀
白色沉淀
现象,则表明残留物已洗净;否则,表明残留物未洗净.(3)有机合成材料:
2011年9月27日第十一届中国塑料交易会在台州市国际会展中心落下帷幕.其中超高分子量聚乙烯制成的防弹背心、防刺手套、聚丙烯制成的奥迪A6保险杠等都是本次塑料交易会重要产品之一.你认为下列制品的主要成分不属于有机合成材料的是
C、F
C、F
(填字母序号)A.聚乙烯制成的防弹背心、防刺手套 B.化学实验室常用的胶皮导管 C.纯棉内衣 D.锦纶制成的尼龙袜子 E. 聚丙烯制成的奥迪A6保险杠 F.真丝围巾.
分析:(1)①了解金属材料及其性质;②正确书写一氧化碳与氧化铁、铁与硫酸铜溶液的反应;掌握铝的性质;
(2)①考虑氢气与氧气可能爆炸,则整个制备过程必须达到无水无氧;
②由生产高纯硅的流程示意图可知,盐酸既是反应物,又是生成物.
③碳酸钙、氧化铁都可与盐酸发生复分解反应;溶液中的氯离子能与硝酸银产生氯化银白色沉淀,滴加硝酸银检验高纯水中是否含氯离子可判断洗净情况;
(3)塑料、合成纤维、合成橡胶就是我们通常所说的三大合成材料.
(2)①考虑氢气与氧气可能爆炸,则整个制备过程必须达到无水无氧;
②由生产高纯硅的流程示意图可知,盐酸既是反应物,又是生成物.
③碳酸钙、氧化铁都可与盐酸发生复分解反应;溶液中的氯离子能与硝酸银产生氯化银白色沉淀,滴加硝酸银检验高纯水中是否含氯离子可判断洗净情况;
(3)塑料、合成纤维、合成橡胶就是我们通常所说的三大合成材料.
解答:解:(1)金属材料:①在下列应用中使用金属材料的有:金、银、铜牌;“鸟巢”;②赤铁矿的主要成分是氧化铁,一氧化碳能与氧化铁在高温条件下反应生成铁和二氧化碳,故填:Fe2O3+3CO
2Fe+3CO2;铁与硫酸铜溶液反应制取铜的化学方程式Fe+CuSO4=FeSO4+Cu;铝的化学性质比较活泼,在常温下能和氧气反应,从而在铝的表面形成一层致密、坚硬的氧化物薄膜,从而阻止了铝和氧气的进一步反应.故填:铝与空气中的氧气反应生成致密的氧化物薄膜,使其不易生锈;
(2)①整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,因为氢气不纯,可能爆炸;故可能引起的后果是硅被氧化得不到高纯硅,且发生爆炸.
②由图知:为了达到绿色化学和资源综合利用的目的,上述生产流程中可以循环使用的物质有其化学式是HCl;
③碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,氧化铁与盐酸反应生成氯化铁和水;向水洗后的溶液中滴加硝酸银,如果出现白色沉淀说明溶液中含有氯离子,表明残留物未洗净,如果不出现沉淀说明溶液中不含氯离子,表明残留物洗净.故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O(或Fe2O3+6HCl═2FeCl3+3H2O);白色沉淀;
(3)人们通常所说的三大合成材料是指塑料、合成纤维、合成橡胶.主要成分属于有机合成材料:A.聚乙烯制成的防弹背心、防刺手套 B.化学实验室常用的胶皮导管 D.锦纶制成的尼龙袜子 E. 聚丙烯制成的奥迪A6保险杠;主要成分不属于有机合成材料为:C.纯棉内衣 F.真丝围巾.故选C、F.
故答案为:(1)①A、C.②Fe2O3+3CO
2Fe+3CO2; Fe+CuSO4=FeSO4+Cu;
铝与空气中的氧气反应生成致密的氧化物薄膜,使其不易生锈.
(2)①氢气不纯,可能爆炸.②稀盐酸.③CaCO3+2HCl═CaCl2+CO2↑+H2O 白色沉淀;
(3)C、F
| ||
(2)①整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,因为氢气不纯,可能爆炸;故可能引起的后果是硅被氧化得不到高纯硅,且发生爆炸.
②由图知:为了达到绿色化学和资源综合利用的目的,上述生产流程中可以循环使用的物质有其化学式是HCl;
③碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,氧化铁与盐酸反应生成氯化铁和水;向水洗后的溶液中滴加硝酸银,如果出现白色沉淀说明溶液中含有氯离子,表明残留物未洗净,如果不出现沉淀说明溶液中不含氯离子,表明残留物洗净.故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O(或Fe2O3+6HCl═2FeCl3+3H2O);白色沉淀;
(3)人们通常所说的三大合成材料是指塑料、合成纤维、合成橡胶.主要成分属于有机合成材料:A.聚乙烯制成的防弹背心、防刺手套 B.化学实验室常用的胶皮导管 D.锦纶制成的尼龙袜子 E. 聚丙烯制成的奥迪A6保险杠;主要成分不属于有机合成材料为:C.纯棉内衣 F.真丝围巾.故选C、F.
故答案为:(1)①A、C.②Fe2O3+3CO
| ||
铝与空气中的氧气反应生成致密的氧化物薄膜,使其不易生锈.
(2)①氢气不纯,可能爆炸.②稀盐酸.③CaCO3+2HCl═CaCl2+CO2↑+H2O 白色沉淀;
(3)C、F
点评:对知识进行迁移解决情形相似的新问题是本题的特点,体现出知识运用与问题分析的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
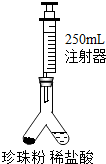 (2013?海安县一模)珍珠粉以其良好的养颜等功效,获得消费者喜爱.资料显示:珍珠中含碳酸钙80-93%、蛋白质4-14%、水份2-4%、十几种氨基酸、28种微量元素.然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠.以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案.
(2013?海安县一模)珍珠粉以其良好的养颜等功效,获得消费者喜爱.资料显示:珍珠中含碳酸钙80-93%、蛋白质4-14%、水份2-4%、十几种氨基酸、28种微量元素.然而一些不法分子用回收的贝壳加上工业用氢氧化钠配制的药水进行清洗、晾晒以后直接加工销售,其主要成分是:碳酸钙,及少量残留氢氧化钠.以下是某化学兴趣小组设计辨别真假珍珠,并测定珍珠中碳酸钙含量的实验探究方案.