题目内容
在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,广泛应用于实际生产和生活中.在工业上,制取氯气的主要工艺流程如下: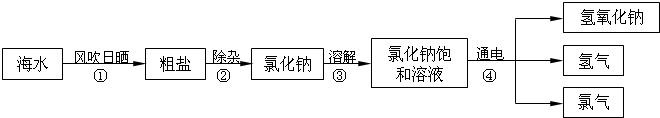
(1)步骤①利用风吹日晒可以从海水中提取粗盐,该过程主要发生
(2)步骤②若要除去食盐水中混有的少量泥沙,可选择的操作方法是
(3)请写出步骤④发生反应的化学方程式
(4)氯气与氢氧化钠溶液反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,工业上用氯气与石灰乳 (Ca(OH)2)反应来制取漂白粉,有关反应的化学方程式是
分析:利用风吹日晒从海水中提取粗盐的过程中,水不断蒸发,氯化钠的质量分数越来越大,没有学位证生成,属于物理变化;过滤可以除去不溶于水的物质;根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式.
解答:解:(1)步骤①利用风吹日晒可以从海水中提取粗盐,该过程主要发生的是物理变化.故填:物理.
(2)若要除去食盐水中混有的少量泥沙,可选择的操作方法是过滤.故填:过滤.
在实验室中该操作所需要的玻璃仪器有:烧杯、玻璃棒、漏斗,玻璃棒在步骤③中的作用是搅拌加速食盐溶解.故填:漏斗;搅拌加速食盐溶解.
(3)电解食盐水的化学方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
该反应不能用于实验室制取氢气,因为生成的气体中含有氯气.故填:不能.
(4)工业上用氯气与石灰乳反应来制取漂白粉,有关反应的化学方程式是:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
(2)若要除去食盐水中混有的少量泥沙,可选择的操作方法是过滤.故填:过滤.
在实验室中该操作所需要的玻璃仪器有:烧杯、玻璃棒、漏斗,玻璃棒在步骤③中的作用是搅拌加速食盐溶解.故填:漏斗;搅拌加速食盐溶解.
(3)电解食盐水的化学方程式为:2NaCl+2H2O
| ||
该反应不能用于实验室制取氢气,因为生成的气体中含有氯气.故填:不能.
(4)工业上用氯气与石灰乳反应来制取漂白粉,有关反应的化学方程式是:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
点评:解答本题要掌握化学方程式的书写方法和过滤等方面的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目

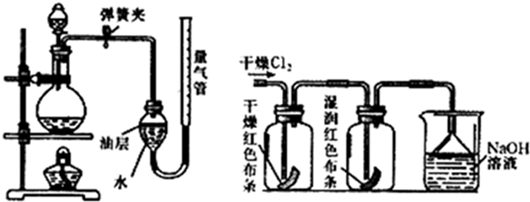
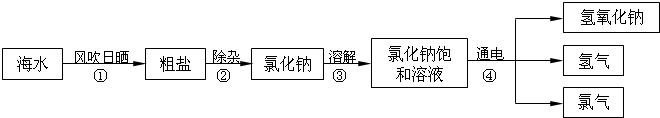
 在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,广泛应用于实际生产和生活中。在工业上,制取氯气的主要工艺流程如下:
在通常状况下,氯气是一种黄绿色气体,密度比空气大,易溶于水,广泛应用于实际生产和生活中。在工业上,制取氯气的主要工艺流程如下: